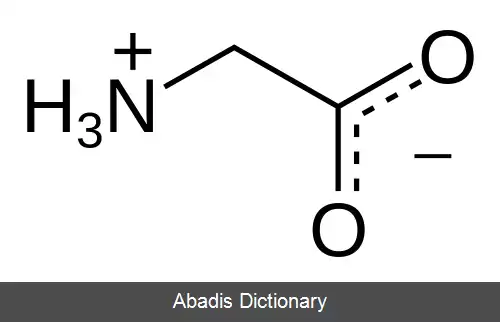
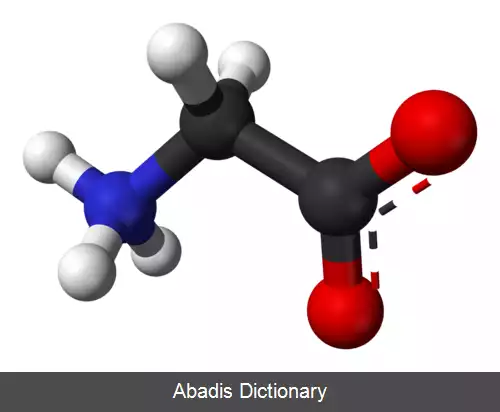
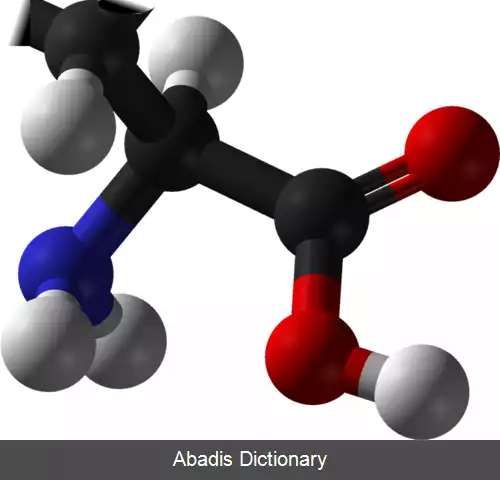
گلایسین یا گلیسین ( به انگلیسی: Glycine ) با نماد Gly یا G ، ساده ترین اسید آمینه پایدار در تمام یاخته های زنده و در بین آمینو اسیدهاست. این اسید آمینه سبک ترین و تنها اسید آمینه ی غیر کایرال است. کدهای ژنتیکی این اسید آمینه عبارتند از: GGU, GGC, GGA و GGG. گلایسین یکی از ۲۰ اسید آمینه پروتئین زا است که پروتئین ها را می سازند. این آمینو اسید آمفی پاتیک است و دارای هر دو سر آب گریز و آب دوست است.
هنری براکونات شیمیدان فرانسوی در سال ۱۸۲۰ گلایسین را با هیدرولیز کردن ژلاتین کشف کرد. وی به منظور هیدرولیز کردن ژلاتین، آن را به همراه سولفوریک اسید جوشاند. [ ۴] در ابتدا او نام ماده به دست آمده را «شکر ژلاتین» نامید[ ۵] [ ۶] اما ژان - بتیست بوسانگو شیمیدان فرانسوی نشان داد که این ماده شامل نیتروژن است. [ ۷] دانشمند آمریکایی Eben Norton Horsford و پس از آن یوستوس فون لیبیش یک دانشجوی شیمی آلمانی، واژه گلیکوکال را پیشنهاد دادند[ ۸] [ ۹] اما یاکوب برسلیوس شیمیدان سوئدی نام ساده تر گلایسین را ارائه داد[ ۱۰] [ ۱۱] این نام از واژه یونانی γλυκύς به معنای شیرین گرفته شده است. [ ۱۲] ( به پیشوندهای glyco - و gluco - نیز ارتباط دارد، مانند گلیکوپروتئین و گلوکز ) . در سال ۱۸۵۸ شیمیدان فرانسوی آگوست آندره توماس کاهورس مشخص کرد که گلایسین، یک آمین از استیک اسید است. [ ۱۳]
گلایسین دارای یک اتم هیدروژن در زنجیر جانبی خود است. به همین دلیل این آمینو اسید پایدار هست و به راحتی به آمینو اسیدهای دیگر تبدیل نمی شود. گلایسین، فراوان ترین آمینو اسید در کلاژن است و همچنین به عنوان یک ناقل عصبی شناخته شده است.
اکثر پروتئین ها مقداری خیلی کمی گلایسین دارند به استثنای گیلاتین و کولاگین که دارای ۲۵–۳۰٪ گلایسین هستند. بدن انسان مقدار زیادی گلایسین نیاز دارد برای اینکه جگر انسان بتواند کارش را به خوبی انجام دهد.
این آمینو اسید غیر قطبی است اما در واکنش های آب گریز شرکت نمی کند. ساختار ساده و کوچک این آمینو اسید و تبادل یک هیدروژن با زنجیره جانبی باعث شده تا در محیط های مختلف خواص اسیدی و بازی متفاوتی از خود نشان دهد.
مواد غذایی انسان و حیوان
اهمیت تغذیه ای گلایسین دلیل استفادهٔ گستردهٔ آن در موادغذایی نیست بلکه به علت خاصیت نگه دارندگی، خوشبو بودن و همچنین شیرینی ملایم این ماده، از آن استفاده می شود و این ماده طعم ناخوشایند ساخارین را از بین می برد. از ترکیب گلایسین و فلزات مانند "گلایسینات مس ( II ) " به عنوان مکمل خوراک دام استفاده می شود. [ ۱۴]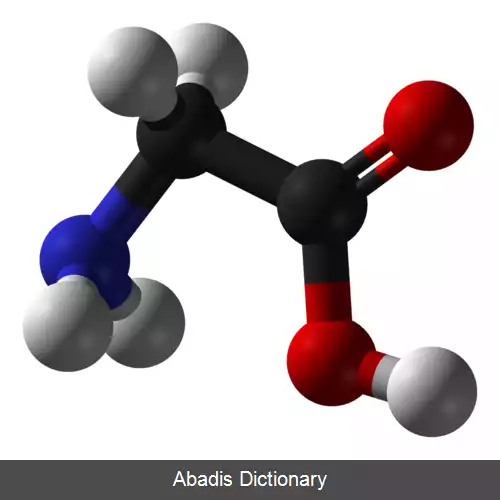
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفهنری براکونات شیمیدان فرانسوی در سال ۱۸۲۰ گلایسین را با هیدرولیز کردن ژلاتین کشف کرد. وی به منظور هیدرولیز کردن ژلاتین، آن را به همراه سولفوریک اسید جوشاند. [ ۴] در ابتدا او نام ماده به دست آمده را «شکر ژلاتین» نامید[ ۵] [ ۶] اما ژان - بتیست بوسانگو شیمیدان فرانسوی نشان داد که این ماده شامل نیتروژن است. [ ۷] دانشمند آمریکایی Eben Norton Horsford و پس از آن یوستوس فون لیبیش یک دانشجوی شیمی آلمانی، واژه گلیکوکال را پیشنهاد دادند[ ۸] [ ۹] اما یاکوب برسلیوس شیمیدان سوئدی نام ساده تر گلایسین را ارائه داد[ ۱۰] [ ۱۱] این نام از واژه یونانی γλυκύς به معنای شیرین گرفته شده است. [ ۱۲] ( به پیشوندهای glyco - و gluco - نیز ارتباط دارد، مانند گلیکوپروتئین و گلوکز ) . در سال ۱۸۵۸ شیمیدان فرانسوی آگوست آندره توماس کاهورس مشخص کرد که گلایسین، یک آمین از استیک اسید است. [ ۱۳]
گلایسین دارای یک اتم هیدروژن در زنجیر جانبی خود است. به همین دلیل این آمینو اسید پایدار هست و به راحتی به آمینو اسیدهای دیگر تبدیل نمی شود. گلایسین، فراوان ترین آمینو اسید در کلاژن است و همچنین به عنوان یک ناقل عصبی شناخته شده است.
اکثر پروتئین ها مقداری خیلی کمی گلایسین دارند به استثنای گیلاتین و کولاگین که دارای ۲۵–۳۰٪ گلایسین هستند. بدن انسان مقدار زیادی گلایسین نیاز دارد برای اینکه جگر انسان بتواند کارش را به خوبی انجام دهد.
این آمینو اسید غیر قطبی است اما در واکنش های آب گریز شرکت نمی کند. ساختار ساده و کوچک این آمینو اسید و تبادل یک هیدروژن با زنجیره جانبی باعث شده تا در محیط های مختلف خواص اسیدی و بازی متفاوتی از خود نشان دهد.
مواد غذایی انسان و حیوان
اهمیت تغذیه ای گلایسین دلیل استفادهٔ گستردهٔ آن در موادغذایی نیست بلکه به علت خاصیت نگه دارندگی، خوشبو بودن و همچنین شیرینی ملایم این ماده، از آن استفاده می شود و این ماده طعم ناخوشایند ساخارین را از بین می برد. از ترکیب گلایسین و فلزات مانند "گلایسینات مس ( II ) " به عنوان مکمل خوراک دام استفاده می شود. [ ۱۴]




wiki: گلایسین
