نافلزها گروهی از عناصر شیمیایی هستند. در جدول تناوبی عناصر فلز، نافلز یا شبه فلز هستند.
نافلزات عبارتند از:
• هیدروژن ( H )
• در گروه ۱۴: کربن ( C )
• در گروه ۱۵: نیتروژن ( N ) ، فسفر ( P )
• در گروه ۱۶: اکسیژن ( O ) ، گوگرد ( S ) ، سلنیوم ( Se )
• در گروه ۱۷: هالوژن ها
• در گروه ۱۸: گازهای نجیب
• • در مقایسه با فلزات، عموماً رسانندهٔ گرما و الکتریسیته نیستند البته برخی از آنها مانند کربن و الماس می توانند به دلیل ساختار بلوری خاص خود به ترتیب جریان الکتریسیته و گرما را از خود عبور دهند.
• • اکسید آن ها خواص اسیدی نشان می دهد، درحالیکه اکسید فلزات خاصیت بازی دارد.
• • در شکل جامد آن ها مات و شکننده هستند، جلای فلزی ندارند، شمش پذیر نیستند و خاصیت چکش خواری ندارند.
• • معمولاً جرم حجمی یا چگالی پایین تری نسبت به فلزات دارند.
• • به طور قابل توجهی دمای ذوب و جوش پایین تری نسبت به فلزات دارند.
• • نافلزات خاصیت تمایل الکترون گیری ( الکترونگاتیویته ) بالاتری دارند.
• • حالت عمومی آنها گازی می باشد که البته برم نافلزی مایع و گوگرد، فسفر، ید، سلنیم و کربن حالت جامد دارند.
• • در واکنش های شیمیایی تمایل به گرفتن الکترون و تشکیل آنیون ویا به اشتراک گذاشتن الکترون را دارند.
این عناصر از نظر تعداد اتم در مولکول هایشان به سه دسته نافلزات چند اتمی، نافلزات دو اتمی و و گازهای نجیب تقسیم می شوند.
این نافلزات شامل عناصر کربن و سلنیم و گوگرد و فسفر است.
تمامی این نافلزات در دمای اتاق به حالت جامدند. این عناصر مولکولهایی بیش از دواتم تشکیل می دهند. کربن می تواند جامدهای کووالانسی غول آسایی مانند گرافیت و الماس بسازد. این عناصر نسبت به گروه بالا رسانای بهتری برای برق اند مثلاً گرافیت یک ماده نیمه رساناست. این گروه نسبت به گروه اول عدد الکترونگاتیوی کمتری دارند و بنا راین بیشتر تمایل دارند تا الکترون های خود را به اشتراک بگذارند و پیوند کووالانسی تشکیل دهند اگر چه عدد الکترونگاتیوی آن ها نسبت به فلزات بسیار بیشتر است. این گروه در ایجاد چرخه حیات بسیار نقش مهمی دارند و کربن ماده اصلی سازنده مولکول های زیستی است. این گروه دمای ذوب و جوش بسیار بالاتری نسبت به گروه دوم دارند.
این نافلزات شامل نه عنصر یعنی تمامی هالوژن ها و عناصر دو اتمی اکسیژن و نیتروژن و هیدروژن است. این عناصر رسانای بسیار ضعیف برق اند ولی بسیار الکترونگاتیو بوده و در ترکیبات یونی پیوندهای محکمی تشکیل می دهند. نکته دیگر این است که از میان این عناصر برم به حالت مایع و ید به حالت جامد در دمای اتاقند.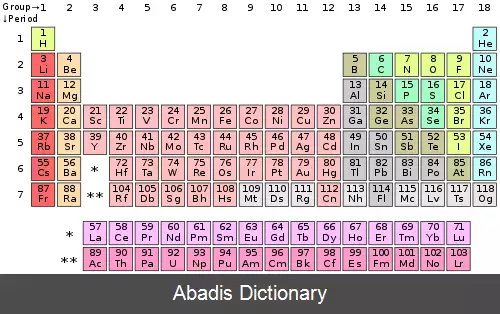



این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفنافلزات عبارتند از:
• هیدروژن ( H )
• در گروه ۱۴: کربن ( C )
• در گروه ۱۵: نیتروژن ( N ) ، فسفر ( P )
• در گروه ۱۶: اکسیژن ( O ) ، گوگرد ( S ) ، سلنیوم ( Se )
• در گروه ۱۷: هالوژن ها
• در گروه ۱۸: گازهای نجیب
• • در مقایسه با فلزات، عموماً رسانندهٔ گرما و الکتریسیته نیستند البته برخی از آنها مانند کربن و الماس می توانند به دلیل ساختار بلوری خاص خود به ترتیب جریان الکتریسیته و گرما را از خود عبور دهند.
• • اکسید آن ها خواص اسیدی نشان می دهد، درحالیکه اکسید فلزات خاصیت بازی دارد.
• • در شکل جامد آن ها مات و شکننده هستند، جلای فلزی ندارند، شمش پذیر نیستند و خاصیت چکش خواری ندارند.
• • معمولاً جرم حجمی یا چگالی پایین تری نسبت به فلزات دارند.
• • به طور قابل توجهی دمای ذوب و جوش پایین تری نسبت به فلزات دارند.
• • نافلزات خاصیت تمایل الکترون گیری ( الکترونگاتیویته ) بالاتری دارند.
• • حالت عمومی آنها گازی می باشد که البته برم نافلزی مایع و گوگرد، فسفر، ید، سلنیم و کربن حالت جامد دارند.
• • در واکنش های شیمیایی تمایل به گرفتن الکترون و تشکیل آنیون ویا به اشتراک گذاشتن الکترون را دارند.
این عناصر از نظر تعداد اتم در مولکول هایشان به سه دسته نافلزات چند اتمی، نافلزات دو اتمی و و گازهای نجیب تقسیم می شوند.
این نافلزات شامل عناصر کربن و سلنیم و گوگرد و فسفر است.
تمامی این نافلزات در دمای اتاق به حالت جامدند. این عناصر مولکولهایی بیش از دواتم تشکیل می دهند. کربن می تواند جامدهای کووالانسی غول آسایی مانند گرافیت و الماس بسازد. این عناصر نسبت به گروه بالا رسانای بهتری برای برق اند مثلاً گرافیت یک ماده نیمه رساناست. این گروه نسبت به گروه اول عدد الکترونگاتیوی کمتری دارند و بنا راین بیشتر تمایل دارند تا الکترون های خود را به اشتراک بگذارند و پیوند کووالانسی تشکیل دهند اگر چه عدد الکترونگاتیوی آن ها نسبت به فلزات بسیار بیشتر است. این گروه در ایجاد چرخه حیات بسیار نقش مهمی دارند و کربن ماده اصلی سازنده مولکول های زیستی است. این گروه دمای ذوب و جوش بسیار بالاتری نسبت به گروه دوم دارند.
این نافلزات شامل نه عنصر یعنی تمامی هالوژن ها و عناصر دو اتمی اکسیژن و نیتروژن و هیدروژن است. این عناصر رسانای بسیار ضعیف برق اند ولی بسیار الکترونگاتیو بوده و در ترکیبات یونی پیوندهای محکمی تشکیل می دهند. نکته دیگر این است که از میان این عناصر برم به حالت مایع و ید به حالت جامد در دمای اتاقند.




wiki: نافلزها
