کشش سطحی ویژگی ای در مایع ها است که باعث می شود لایه بیرونی آن ها به صورت ورقه ای کشسان عمل کند. این همان ویژگی ای است که موجب ربایش دو سطح مایع به یکدیگر می شود؛ مانند دو قطرهٔ آب که همدیگر را می ربایند و قطرهٔ بزرگ تری می سازند. کشش سطحی کمیتی است که بعد نیرو در واحد طول یا انرژی در واحد سطح دارد و در فیزیک معمولاً با γ نشان داده می شود. کشش سطحی را همچنین می توان مقدار کار لازم برای ایجاد واحد سطح مشترک جدید در نظر گرفت.
هر مولکول مایع از سوی مولکول های دیگرِ مایع ربوده می شود. مولکول هایی که درون حجم مایع هستند، از همه جهت ربوده می شوند و برآیند نیروی وارد به آن ها صفر است. اما مولکول هایی که در سطح مایع هستند، تنها از یک جهت از سوی دیگر مولکول ها ربوده می شوند و نیروی ربایش در آن سوی مرز مایع ( مثلاً از طرف مولکول های هوا ) به آن ها کمتر است؛ بنابراین، به مولکول های روی سطح مایع نیروی خالصی به سمت درون وارد می شود که این نیرو با مقاومت مایع در برابر فشرده شدن خنثی می شود. در نتیجه، نیرویی در مایع به وجود می آید که می خواهد سطح مایع را کم کند. از همین رو سطح مایع به شکل ورقه ای الاستیک عمل می کند و آن قدر جمع می شود که کمترین سطح ممکن را داشته باشد.
راه دیگر برای توضیح کشش سطحی این است که یک مولکول اگر در کنار مولکول همسایه اش باشد، انرژی اش کمتر از وقتی است که کنار آن همسایه نباشد. مولکول های درونی بیشترین تعداد همسایه های ممکن را دارند؛ ولی مولکول هایی که در سطح هستند همسایه های کمتری دارند و بنابراین انرژی شان بیشتر از انرژی مولکول های درونی است؛ بنابراین، وقتی که مایع می خواهد انرژی کلش را کمینه کند، می کوشد تا از شمار مولکول های سطحی اش بکاهد، و این یعنی یک مایع می خواهد کمترین سطح ممکن را داشته باشد.
برای کاستن از سطح، یک مایع همیشه هموارترین شکل ممکن را در سطح خود می گیرد ( اثبات ریاضی این که چرا هموارترین سطح متناظر است با کمترین مساحت نیازمند قضیهٔ اویلر - لاگرانژ است ) . هر خمیدگی تازه بر روی سطح به مساحت بیشتر و در نتیجه انرژی بیشتر می انجامد.
در واقع علت ایجاد سطح مقاوم به نیرو در سطح مایعات مقاومت مایع در برابر تغییر مساحت خارجی است
زیرا مایع تمایل دارد در حالت سطح کمینه باقی بماند دلیل دیگر مقاومت نیروهای بین مولکولی سطح ( واندروالسی ) در برابر فاصله گرفتن از هم است



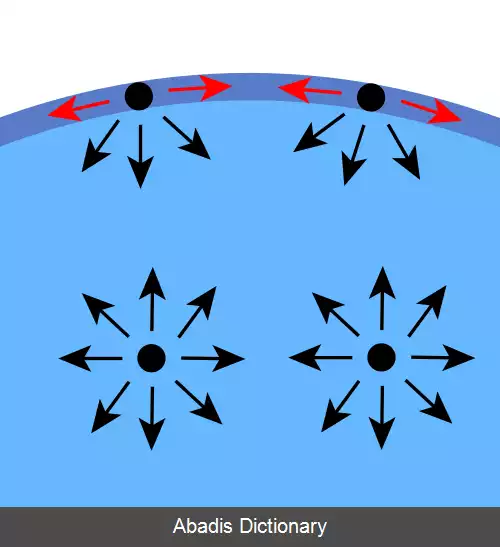

این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفهر مولکول مایع از سوی مولکول های دیگرِ مایع ربوده می شود. مولکول هایی که درون حجم مایع هستند، از همه جهت ربوده می شوند و برآیند نیروی وارد به آن ها صفر است. اما مولکول هایی که در سطح مایع هستند، تنها از یک جهت از سوی دیگر مولکول ها ربوده می شوند و نیروی ربایش در آن سوی مرز مایع ( مثلاً از طرف مولکول های هوا ) به آن ها کمتر است؛ بنابراین، به مولکول های روی سطح مایع نیروی خالصی به سمت درون وارد می شود که این نیرو با مقاومت مایع در برابر فشرده شدن خنثی می شود. در نتیجه، نیرویی در مایع به وجود می آید که می خواهد سطح مایع را کم کند. از همین رو سطح مایع به شکل ورقه ای الاستیک عمل می کند و آن قدر جمع می شود که کمترین سطح ممکن را داشته باشد.
راه دیگر برای توضیح کشش سطحی این است که یک مولکول اگر در کنار مولکول همسایه اش باشد، انرژی اش کمتر از وقتی است که کنار آن همسایه نباشد. مولکول های درونی بیشترین تعداد همسایه های ممکن را دارند؛ ولی مولکول هایی که در سطح هستند همسایه های کمتری دارند و بنابراین انرژی شان بیشتر از انرژی مولکول های درونی است؛ بنابراین، وقتی که مایع می خواهد انرژی کلش را کمینه کند، می کوشد تا از شمار مولکول های سطحی اش بکاهد، و این یعنی یک مایع می خواهد کمترین سطح ممکن را داشته باشد.
برای کاستن از سطح، یک مایع همیشه هموارترین شکل ممکن را در سطح خود می گیرد ( اثبات ریاضی این که چرا هموارترین سطح متناظر است با کمترین مساحت نیازمند قضیهٔ اویلر - لاگرانژ است ) . هر خمیدگی تازه بر روی سطح به مساحت بیشتر و در نتیجه انرژی بیشتر می انجامد.
در واقع علت ایجاد سطح مقاوم به نیرو در سطح مایعات مقاومت مایع در برابر تغییر مساحت خارجی است
زیرا مایع تمایل دارد در حالت سطح کمینه باقی بماند دلیل دیگر مقاومت نیروهای بین مولکولی سطح ( واندروالسی ) در برابر فاصله گرفتن از هم است






wiki: کشش سطحی
