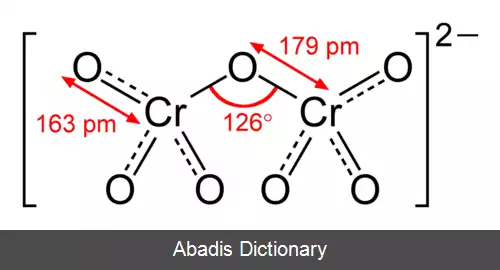
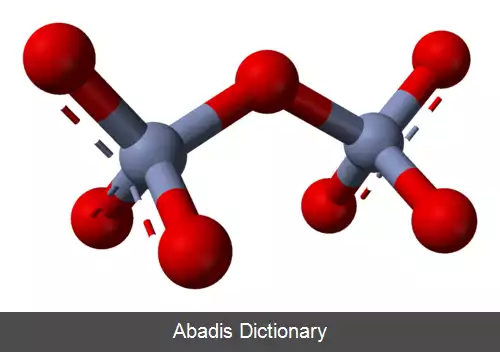
کرومات ( به انگلیسی: Chromate ) یک آنیون چند اتمی با فرمول شیمیاییCrO2−4 و دی کرومات ( به انگلیسی: dichromate ) یک آنیون چند اتمی با فرمول شیمیایی Cr2O2−7 است. در این اکسی آنیون ها اتم کروم در حالت اکسایش ۶+ می باشد. ترکیبات یونی حاوی این دو آنیون جز عوامل اکسید کننده نسبتاً قوی به شمار می روند. در محلول های آبی، یون کرومات و دی کرومات می توانند به صورت برگشت پذیر به هم ترادیسیده ( تبدیل ) شوند.
کرومات ها با هیدروژن پراکسید واکنش نشان می دهند و فرآورده هایی را می سازند که در آنها یون پراکسید ( O2−2 ) جایگزین یک یا چند اتم اکسیژن می شود. در محلول اسید، کمپلکس ناپایدار آبی پراوکسو کروم ( VI ) اکسید پراکسید، CrO ( O2 ) 2 ساخته می شود. این کمپلکس یک مولکول کووالانسی بی بار است، که ممکن است در اتر استخراج شود. با افزودن پیریدین، کمپلکس پایدارتر CrO ( O2 ) 2py شکل می گیرد.
در محلول آبی، آنیون های کرومات و دی کرومات در تعادل شیمیایی می باشند.

این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفکرومات ها با هیدروژن پراکسید واکنش نشان می دهند و فرآورده هایی را می سازند که در آنها یون پراکسید ( O2−2 ) جایگزین یک یا چند اتم اکسیژن می شود. در محلول اسید، کمپلکس ناپایدار آبی پراوکسو کروم ( VI ) اکسید پراکسید، CrO ( O2 ) 2 ساخته می شود. این کمپلکس یک مولکول کووالانسی بی بار است، که ممکن است در اتر استخراج شود. با افزودن پیریدین، کمپلکس پایدارتر CrO ( O2 ) 2py شکل می گیرد.
در محلول آبی، آنیون های کرومات و دی کرومات در تعادل شیمیایی می باشند.




wiki: کرومات و دی کرومات
