در شیمی، دایریلتن نام عمومی از یک کلاس از ترکیبات شیمیایی که خصلت آروماتیکی داشته و متصل به انتهای یک کربن - کربن پیوند دوگانههستند. ساده ترین مثال استیلبن است که دارای دو ایزومر سیس - ترانس E و Z است.
تحت تأثیر نور، این ترکیبات به طور کلی می توانند دو نوع ایزومریزاسیون قابل برگشت را انجام دهند:[ ۱]
• ایزومریزاسیون های E تا Z، در بین استیلبن ها ( و آزوبنزنها ) معمول است. این فرایند از کمینه شدن انرژی حالت برانگیخته جایی که حلقه های آروماتیک در حالت ۹۰ درجه یکدیگر قرار دارند جریان دارد. این ترکیب به حالت پایه رفته و به طور کلی به فرم های ترانس و سیس در نسبت ۱: ۱ بهینه می شود، بنابراین بازده کوانتومی برای ایزومریزاسیون E−Z به ندرت از ۵/۰ بیشتر است.
• واکنش الکتروسیکلیک ۶π از فرم Z، منجر به پیوند اضافه بین دو ویژگی آریل و ضریب پخش خصلت آروماتیک این گروه ها می شود. [ ۲] بازده کوانتومی این واکنش به طور کلی کمتر از ۰٫۱ است و در اکثر دایریلتن ها شکل حلقه بسته از نظر دمایی ناپایدار است و در مدت زمان چند ثانیه یا چند دقیقه در شرایط محیط به حالت همسو ( CIS ) برمی گردد.
همپاری های ( ایزومراسیون ) حرارتی نیز ممکن است. در ایزومریزاسیون EZ، تعادل حرارتی بخاطر انرژی کمتری که دارد ( ۱۵ کیلو ژول مول - 1 در استیلبن ) به سمت ناهمسو شکل می یابد. [ ۳] انرژی فعال سازی برای ایزومریزاسیون EZ حرارتی ۱۵۰–۱۹۰ کیلوژول مول - 1 برای استیلبن است، به این معنی که درجه حرارت بالاتر از ۲۰۰ درجه سانتیگراد برای ایزومریزه کردن استیلبن با یک نرخ معقول مورد نیاز است، اما بیشتر مشتقات سد انرژی کمتری دارند ( به عنوان مثال ۶۵ کیلوژول مول - 1 برای ۴ - آمینوستیلبن ) . انرژی فعال سازی الکتروسیکلیزاسیون ۷۳ کیلوژول مول - 1 برای استیلبن است.
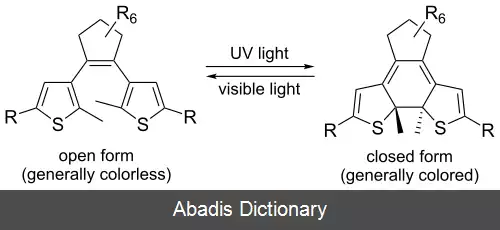
هر دو فرایند اغلب در سوئیچ های مولکولی و برای فوتوکرومیسم ( تغییر حالت برگشت پذیر برآمده از قرار گرفتن در معرض نور ) استفاده می شوند. [ ۴] [ ۵] [ ۶]
پس از الکتروکایزاسیون ۶π از فرم Z به فرم «حلقه بسته»، اکثر دیاریلنهای ناجانشنین مستعد اکسیداسیونهستند و منجر به آروماتیک سازی مجدد سیستم π می شوند. متداول ترین نمونه استیلبن ئیاست که پس از تابش از ایزومریزاسیون E تا Z استفاده می شود، که می تواند با استفاده از الکتروسیکلیزاسیون ۶π دنبال شود. واکنش محصول این واکنش با اکسیژن مولکولی، فنانترن را فراهم می کند، و توسط برخی مطالعات پیشنهاد شده است که هیدروژن زدایی حتی ممکن است به صورت خودبخود رخ دهد. واسطه دیهدروفناترن هرگز جدا نشده است، اما با توجه به باند جذب نوری طول موج بلند آن، در آزمایش های پمپ روبشی طیف سنجی تشخیص داده شده است. اگرچه هم ایزومریزاسیون EZ و هم الکترولیزاسیون ۶π فرایندهای برگشت پذیر هستند، اما این اکسیداسیون کل توالی را غیرقابل برگشت می کند. [ ۲]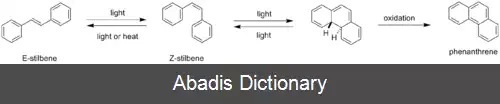
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفتحت تأثیر نور، این ترکیبات به طور کلی می توانند دو نوع ایزومریزاسیون قابل برگشت را انجام دهند:[ ۱]
• ایزومریزاسیون های E تا Z، در بین استیلبن ها ( و آزوبنزنها ) معمول است. این فرایند از کمینه شدن انرژی حالت برانگیخته جایی که حلقه های آروماتیک در حالت ۹۰ درجه یکدیگر قرار دارند جریان دارد. این ترکیب به حالت پایه رفته و به طور کلی به فرم های ترانس و سیس در نسبت ۱: ۱ بهینه می شود، بنابراین بازده کوانتومی برای ایزومریزاسیون E−Z به ندرت از ۵/۰ بیشتر است.
• واکنش الکتروسیکلیک ۶π از فرم Z، منجر به پیوند اضافه بین دو ویژگی آریل و ضریب پخش خصلت آروماتیک این گروه ها می شود. [ ۲] بازده کوانتومی این واکنش به طور کلی کمتر از ۰٫۱ است و در اکثر دایریلتن ها شکل حلقه بسته از نظر دمایی ناپایدار است و در مدت زمان چند ثانیه یا چند دقیقه در شرایط محیط به حالت همسو ( CIS ) برمی گردد.
همپاری های ( ایزومراسیون ) حرارتی نیز ممکن است. در ایزومریزاسیون EZ، تعادل حرارتی بخاطر انرژی کمتری که دارد ( ۱۵ کیلو ژول مول - 1 در استیلبن ) به سمت ناهمسو شکل می یابد. [ ۳] انرژی فعال سازی برای ایزومریزاسیون EZ حرارتی ۱۵۰–۱۹۰ کیلوژول مول - 1 برای استیلبن است، به این معنی که درجه حرارت بالاتر از ۲۰۰ درجه سانتیگراد برای ایزومریزه کردن استیلبن با یک نرخ معقول مورد نیاز است، اما بیشتر مشتقات سد انرژی کمتری دارند ( به عنوان مثال ۶۵ کیلوژول مول - 1 برای ۴ - آمینوستیلبن ) . انرژی فعال سازی الکتروسیکلیزاسیون ۷۳ کیلوژول مول - 1 برای استیلبن است.
هر دو فرایند اغلب در سوئیچ های مولکولی و برای فوتوکرومیسم ( تغییر حالت برگشت پذیر برآمده از قرار گرفتن در معرض نور ) استفاده می شوند. [ ۴] [ ۵] [ ۶]
پس از الکتروکایزاسیون ۶π از فرم Z به فرم «حلقه بسته»، اکثر دیاریلنهای ناجانشنین مستعد اکسیداسیونهستند و منجر به آروماتیک سازی مجدد سیستم π می شوند. متداول ترین نمونه استیلبن ئیاست که پس از تابش از ایزومریزاسیون E تا Z استفاده می شود، که می تواند با استفاده از الکتروسیکلیزاسیون ۶π دنبال شود. واکنش محصول این واکنش با اکسیژن مولکولی، فنانترن را فراهم می کند، و توسط برخی مطالعات پیشنهاد شده است که هیدروژن زدایی حتی ممکن است به صورت خودبخود رخ دهد. واسطه دیهدروفناترن هرگز جدا نشده است، اما با توجه به باند جذب نوری طول موج بلند آن، در آزمایش های پمپ روبشی طیف سنجی تشخیص داده شده است. اگرچه هم ایزومریزاسیون EZ و هم الکترولیزاسیون ۶π فرایندهای برگشت پذیر هستند، اما این اکسیداسیون کل توالی را غیرقابل برگشت می کند. [ ۲]


wiki: دایریلتن
