ترکیب آلی کادمیوم. ترکیب آلی کادمیم یک ترکیب در شیمی آلی فلزی است که دارای پیوند کربن - کادمیم است. شیمی آلی کادمیم ویژگی های فیزیکی، تولید و واکنش های این پیوندهای شیمیایی را توضیح می دهد. [ ۱] کادمیم همانند جیوه و روی در گروه ۱۲ جدول تناوبی است از این رو ویژگی های شیمیایی همانند این دو عنصر دارد.
دی متیل کادمیم دارای مولکول های خطی با پیوند C - Cd است که طول پیوند آن ۲۱۳ پیکومتر است[ ۲] همهٔ ترکیبات آلی کادمیم نسبت به هوا، نور و رطوبت حساس اند.
نخستین ترکیب تولیدی آلی کادمیم، دی متیل کادمیم، CH3 - Cd - CH3 و دی اتیل کادمیم CH3CH2 - Cd - CH2CH3 است که نخستین بار در سال ۱۹۱۷ از سوی اریک کروز تولید شدند. این سنتز با کمک یک واکنش تبادلی میان یک واکنشگر ناب آلی فلزی و یک نمک کادمیم ایجاد می شود. [ ۳]
یک فرایند در تولید دی اتیل کادمیم واکنش میان کادمیم برومید با دو واکنشگر گرینیارد معادل اتیل منیزیم برومید در دی اتیل اتر است. یک محصول جانبی واکنش برمید منیزیم است. دی اتیل کادمیم روغنی بی رنگ با نقطهٔ ذوب ۲۱ - درجهٔ سلسیوس است.
دی فنیل کادمیم را می توان از واکنش میان فنیل لیتیم با کادمیم برمید بدست آورد. دی فنیل کادمیم جامد و نقطهٔ ذوب آن ۱۷۴ درجهٔ سانتیگراد است.
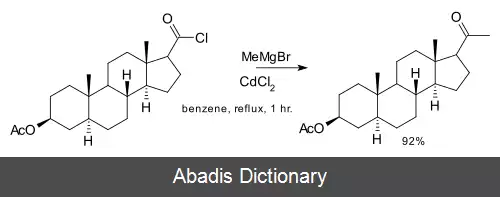
کاربرد ترکیب های آلی کادمیم محدود است. در گروه آلکیل ها هسته دوستی کمتری دیده می شود تا در ترکیبات آلی روی چون با پایین رفتن در گروه ۱۲ میزان الکترونگاتیوی کمتر می شود. یکی از نمونه های خوب کاربرد ترکیب های آلی کادمیم، استفاده از متیل کادمیم در یکی از گام های تولید کلسترول است:[ ۴]
ترکیب های کادمیم همه سمی دانسته می شوند. دی متیل کادمیم به کلیه، کبد، دستگاه عصبی و تنفسی آسیب رسان است. [ ۵] مرکز جهانی تحقیقات سرطان، همهٔ ترکیب های کادمیم را سرطان زا اعلام کرده است. [ ۶]
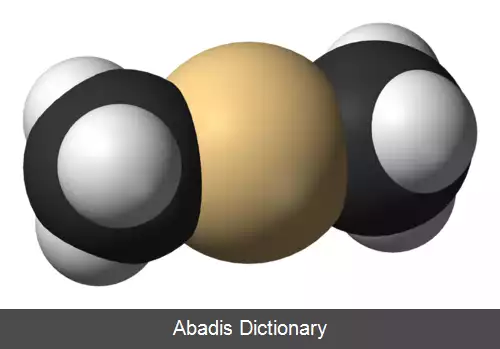
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفدی متیل کادمیم دارای مولکول های خطی با پیوند C - Cd است که طول پیوند آن ۲۱۳ پیکومتر است[ ۲] همهٔ ترکیبات آلی کادمیم نسبت به هوا، نور و رطوبت حساس اند.
نخستین ترکیب تولیدی آلی کادمیم، دی متیل کادمیم، CH3 - Cd - CH3 و دی اتیل کادمیم CH3CH2 - Cd - CH2CH3 است که نخستین بار در سال ۱۹۱۷ از سوی اریک کروز تولید شدند. این سنتز با کمک یک واکنش تبادلی میان یک واکنشگر ناب آلی فلزی و یک نمک کادمیم ایجاد می شود. [ ۳]
یک فرایند در تولید دی اتیل کادمیم واکنش میان کادمیم برومید با دو واکنشگر گرینیارد معادل اتیل منیزیم برومید در دی اتیل اتر است. یک محصول جانبی واکنش برمید منیزیم است. دی اتیل کادمیم روغنی بی رنگ با نقطهٔ ذوب ۲۱ - درجهٔ سلسیوس است.
دی فنیل کادمیم را می توان از واکنش میان فنیل لیتیم با کادمیم برمید بدست آورد. دی فنیل کادمیم جامد و نقطهٔ ذوب آن ۱۷۴ درجهٔ سانتیگراد است.
کاربرد ترکیب های آلی کادمیم محدود است. در گروه آلکیل ها هسته دوستی کمتری دیده می شود تا در ترکیبات آلی روی چون با پایین رفتن در گروه ۱۲ میزان الکترونگاتیوی کمتر می شود. یکی از نمونه های خوب کاربرد ترکیب های آلی کادمیم، استفاده از متیل کادمیم در یکی از گام های تولید کلسترول است:[ ۴]
ترکیب های کادمیم همه سمی دانسته می شوند. دی متیل کادمیم به کلیه، کبد، دستگاه عصبی و تنفسی آسیب رسان است. [ ۵] مرکز جهانی تحقیقات سرطان، همهٔ ترکیب های کادمیم را سرطان زا اعلام کرده است. [ ۶]



wiki: ترکیب آلی کادمیوم
