پیوندپوشی یا هاپتیسیته ، ( به انگلیسی: Hapticity ) به کوردیناسیون فلز مرکزی توسط اتم های همسایه در یک لیگاند گفته می شود. پیوندپوشی بیشتر در میان ترکیبات ساندویچی در شیمی آلی فلزی دیده می شود.
پیوندپوشی با علامت η ( اتا و یک عدد که به صورت بالانویس بیانگر تعداد اتم های همسایه است، نشان داده می شود. برای نمونه η2 نشان دهنده این است که دو اتم همسایه با اتم مرکزی در پیوند هستند.
دو نماد نویسی دیگر برای دندانگی ( κ ) و پل ( μ ) نیز وجود دارد.
ممکن است پیوندپوشی در یک واکنش مانند اکسایش - کاهش تغییر کند.
برای نمونه:
که در آن روتنیوم پس از واکنش تنها با چهار اتم همسایه از لیگاند آروماتیک بالایی پیوندپوشی شده است.
پیوندپوشی مفهومی کاملاً متفاوت با دندانگی است. در دندانگی پیوند از سایت های مشخصی برقرار می گردد، اما در پیوندپوشی مستقیماً خود اتم ها وارد پیوند می شوند.
• W ( CO ) 3 ( PiPr3 ) 2 ( η2 - H2 ) [ ۱] [ ۲]
• K. H2O
• ( μ - η2:η2 - C2H2 ) Co2 ( CO ) 6 and ( Cp*2Sm ) 2 ( μ - η2:η2 - N2 ) [ ۳]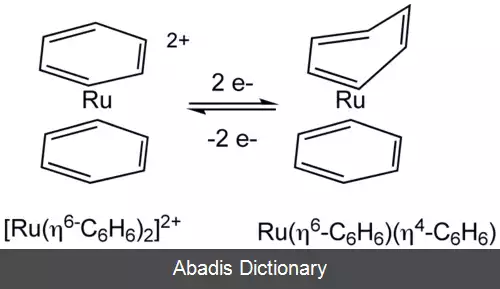
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفپیوندپوشی با علامت η ( اتا و یک عدد که به صورت بالانویس بیانگر تعداد اتم های همسایه است، نشان داده می شود. برای نمونه η2 نشان دهنده این است که دو اتم همسایه با اتم مرکزی در پیوند هستند.
دو نماد نویسی دیگر برای دندانگی ( κ ) و پل ( μ ) نیز وجود دارد.
ممکن است پیوندپوشی در یک واکنش مانند اکسایش - کاهش تغییر کند.
برای نمونه:
که در آن روتنیوم پس از واکنش تنها با چهار اتم همسایه از لیگاند آروماتیک بالایی پیوندپوشی شده است.
پیوندپوشی مفهومی کاملاً متفاوت با دندانگی است. در دندانگی پیوند از سایت های مشخصی برقرار می گردد، اما در پیوندپوشی مستقیماً خود اتم ها وارد پیوند می شوند.
• W ( CO ) 3 ( PiPr3 ) 2 ( η2 - H2 ) [ ۱] [ ۲]
• K. H2O
• ( μ - η2:η2 - C2H2 ) Co2 ( CO ) 6 and ( Cp*2Sm ) 2 ( μ - η2:η2 - N2 ) [ ۳]

wiki: پیوندپوشی
