پتانسیل لنارد - جونز یک پتانسیل تقریبی برای توصیف برهم کنش میان دو ذره ( اتم یا مولکول ) است که در فاصله های دور نیروی رباینده و در فاصله های نزدیک نیروی راننده دارند. نیروی رباینده معولاً نیروی واندروالسی و نیروی راننده نیروی رانش ناشی از هم پوشانی ابر الکترونی دو ذره است ( نیروی پاؤلی که از اصل طرد پاولی می آید ) . رابطهٔ ریاضی این پتانسیل به شکل زیر است:
V ( r ) = 4 ϵ
در این رابطه ϵ نشان گر عمق چاه پتانسیل است و σ فاصله ای است که در آن پتانسیل صفر می شود. این پارامترها را معمولاً با برازش داده های آزمایشگاهی تعیین می کنند یا از محاسبات دقیق در شیمی کوانتومی به دست می آورند.
پتانسیل لنارد - جونز را گاهی پتانسیل L - J یا پتانسیل ۶ - ۱۲ هم می نامند. این پتانسیل را جان لنارد - جونز در سال 1924 پیشنهاد کرد. [ ۱]
این پتانسیل فقط یک تقریب است و از نظریهٔ بنیادی تری به دست نیامده است. توان ۱۲ در جملهٔ نخست فقط برای افزایش سرعت محاسبات برگزیده شده ( r 12 توان دوم r 6 است ) . با این حال، پتانسیل لنارد - جونز به خاطر سادگی اش اغلب برای مدل سازی خواص گازها و مولکول ها به کار می رود و تقریب خوبی به ویژه برای گازهای نجیب است.
روش های تازه تری نیز برای توصیف دقیق تر برهمکنش میان مولکول ها پیشنهاد شده اند مانند معادلهٔ استوک - میر یا معادلهٔ چندگانه. روش های شیمی کوانتومی مانند نظریهٔ اختلال مولر - پلِسِت، روش خوشهٔ جفتیده یا پتانسیل کامل برهمکنش به نتایج بسیار دقیق تری می انجامند، ولی توان محاسباتی بیشتری را نیز می طلبند.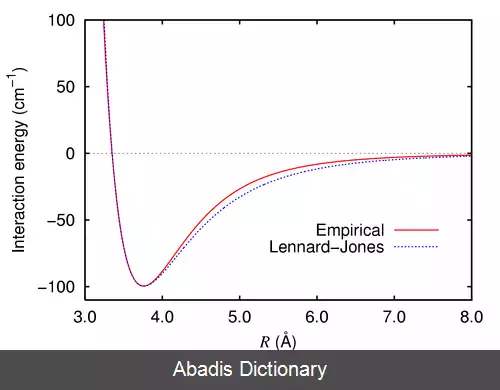
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفV ( r ) = 4 ϵ
در این رابطه ϵ نشان گر عمق چاه پتانسیل است و σ فاصله ای است که در آن پتانسیل صفر می شود. این پارامترها را معمولاً با برازش داده های آزمایشگاهی تعیین می کنند یا از محاسبات دقیق در شیمی کوانتومی به دست می آورند.
پتانسیل لنارد - جونز را گاهی پتانسیل L - J یا پتانسیل ۶ - ۱۲ هم می نامند. این پتانسیل را جان لنارد - جونز در سال 1924 پیشنهاد کرد. [ ۱]
این پتانسیل فقط یک تقریب است و از نظریهٔ بنیادی تری به دست نیامده است. توان ۱۲ در جملهٔ نخست فقط برای افزایش سرعت محاسبات برگزیده شده ( r 12 توان دوم r 6 است ) . با این حال، پتانسیل لنارد - جونز به خاطر سادگی اش اغلب برای مدل سازی خواص گازها و مولکول ها به کار می رود و تقریب خوبی به ویژه برای گازهای نجیب است.
روش های تازه تری نیز برای توصیف دقیق تر برهمکنش میان مولکول ها پیشنهاد شده اند مانند معادلهٔ استوک - میر یا معادلهٔ چندگانه. روش های شیمی کوانتومی مانند نظریهٔ اختلال مولر - پلِسِت، روش خوشهٔ جفتیده یا پتانسیل کامل برهمکنش به نتایج بسیار دقیق تری می انجامند، ولی توان محاسباتی بیشتری را نیز می طلبند.

wiki: پتانسیل لنارد جونز
