ولتامتری چرخه ای ( به انگلیسی: Cyclic voltammetry ) یکی از انواع روش های اندازه گیری الکتروشیمیایی پتانسیودینامیک می باشد. در یک آزمایش ولتامتری چرخه ای پتانسیل الکترود کارگر به صورت خطی با زمان تغییر می کند. بر خلاف ولتامتری روبش خطی، بعد از رسیدن به یک پتانسیل تعیین شده، پتانسیل الکترود کارگر در جهت عکس تغییر می کند تا به پتانسیل اولیه بازگردد. این چرخه های تغییر پتانسیل می توانند به تعداد دلخواه تکرار شوند. جریان ایجاد شده در الکترود کارگر بر حسب ولتاژ ( پتانسیل الکترود کارگر ) رسم می شود تا نمودار ولتامتری چرخه ای به دست آید. ولتامتری چرخه ای معمولاً برای مطالعه یک نمونه در داخل محلول یا یک ماده آبکاری شده بر روی الکترود کارگر و همچنین برای سنتز الکتروشیمیایی مورد استفاده قرار می گیرد. [ ۱] [ ۲] [ ۳]
در ولتامتری چرخه ای پتانسیل الکترود به صورت خطی بر حسب زمان در فازهای چرخه ای تغییر می کند ( شکل ۲ ) . سرعت تغییر ولتاژ بر حسب زمان در طول هر یک از این فازها با عنوان سرعت روبش شناخته می شود. پتانسیل بین الکترود مرجع و الکترود کارگر اعمال می شود در حالیکه جریان بین الکترود کارگر و الکترود کمکی اندازه گیری می گردد. این داده ها به صورت جریان ( i ) در مقابل پتانسیل اعمال شده ( E، اغلب فقط باعنوان 'پتانسیل' ) رسم می شوند. در شکل ۲ در طول روبش رفت اولیه ( از t0 تا t1 ) به طور فزاینده ای پتانسیل کاهشی اعمال شده است؛ بنابراین با فرض وجود نمونه احیا شونده در سیستم، جریان کاتدی حداقل در مراحل اولیه در طول این دوره زمانی افزایش خواهد یافت. کمی بعد از رسیدن به پتانسیل احیای نمونه جریان کاتدی با کاهش غلظت ذرات احیا شونده کاهش خواهد یافت. اگر زوج ردوکس برگشت پذیر باشند در طی روبش برگشت ( از t1 تا t2 ) نمونه احیا شده شروع به اکسایش محدد کرده و باعث ظهور یک جریان ( جریان آندی ) با قطبیت عکس نسبت به قبل ( روبش رفت ) می شود. هرچه مقدار ذرات جفت ردوکس برگشت پذبر بیشتر باشد شکل پیک اکسایش شباهت بیشتری به پیک احیا خواهد داشت؛ بنابراین داده های ولتامتری چرخه ای اطلاعاتی در مورد پتانسیل های ردوکس و سرعت های واکنش الکتروشیمیایی فراهم می کنند.
مثلاً اگر انتقال الکترون در سطح الکترود کارگر سریع باشد و جریان فقط با نفوذ ذرات نمونه به سمت سطح الکترود محدود شود، در این صورت جریان پیک با ریشه دوم سرعت روبش متناسب خواهد بود. این رابطه با معادله کاترل توصیف می شود. در این حالت، ولتامتری چرخه ای تنها بخش کوچکی از محلول یعنی لایه نفوذ در سطح الکترود را مورد آزمایش قرار می دهد.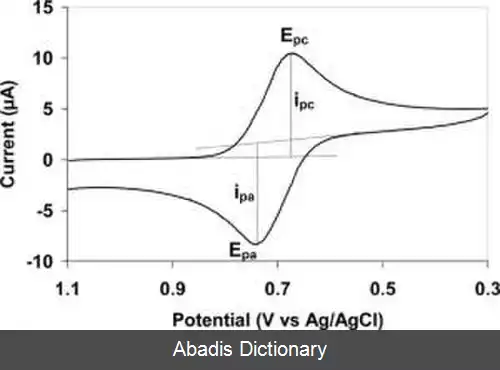
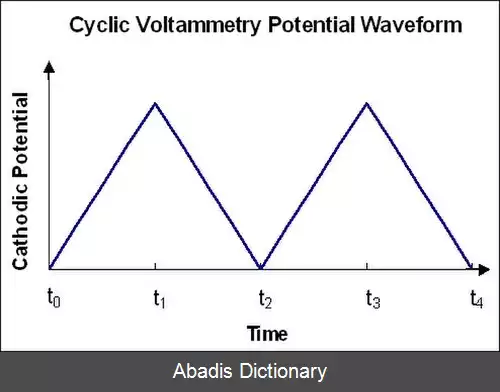
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفدر ولتامتری چرخه ای پتانسیل الکترود به صورت خطی بر حسب زمان در فازهای چرخه ای تغییر می کند ( شکل ۲ ) . سرعت تغییر ولتاژ بر حسب زمان در طول هر یک از این فازها با عنوان سرعت روبش شناخته می شود. پتانسیل بین الکترود مرجع و الکترود کارگر اعمال می شود در حالیکه جریان بین الکترود کارگر و الکترود کمکی اندازه گیری می گردد. این داده ها به صورت جریان ( i ) در مقابل پتانسیل اعمال شده ( E، اغلب فقط باعنوان 'پتانسیل' ) رسم می شوند. در شکل ۲ در طول روبش رفت اولیه ( از t0 تا t1 ) به طور فزاینده ای پتانسیل کاهشی اعمال شده است؛ بنابراین با فرض وجود نمونه احیا شونده در سیستم، جریان کاتدی حداقل در مراحل اولیه در طول این دوره زمانی افزایش خواهد یافت. کمی بعد از رسیدن به پتانسیل احیای نمونه جریان کاتدی با کاهش غلظت ذرات احیا شونده کاهش خواهد یافت. اگر زوج ردوکس برگشت پذیر باشند در طی روبش برگشت ( از t1 تا t2 ) نمونه احیا شده شروع به اکسایش محدد کرده و باعث ظهور یک جریان ( جریان آندی ) با قطبیت عکس نسبت به قبل ( روبش رفت ) می شود. هرچه مقدار ذرات جفت ردوکس برگشت پذبر بیشتر باشد شکل پیک اکسایش شباهت بیشتری به پیک احیا خواهد داشت؛ بنابراین داده های ولتامتری چرخه ای اطلاعاتی در مورد پتانسیل های ردوکس و سرعت های واکنش الکتروشیمیایی فراهم می کنند.
مثلاً اگر انتقال الکترون در سطح الکترود کارگر سریع باشد و جریان فقط با نفوذ ذرات نمونه به سمت سطح الکترود محدود شود، در این صورت جریان پیک با ریشه دوم سرعت روبش متناسب خواهد بود. این رابطه با معادله کاترل توصیف می شود. در این حالت، ولتامتری چرخه ای تنها بخش کوچکی از محلول یعنی لایه نفوذ در سطح الکترود را مورد آزمایش قرار می دهد.


wiki: ولتامتری چرخه ای
