نیروی لاندن ( به انگلیسی: London dispersion force ) از جمله نیروهای ضعیف بین مولکولی است. نوعی جاذبه میان دوقطبی هایی است که بر اثر برهم خوردن توزیع الکترون در مولکول های ناقطبی ایجاد می شود. به این دوقطبی ها القایی می گویند.
برای اینکه ترکیبی به صورت جامد یا مایع باشد. باید نیروهایی، مولکولهای آن ترکیب را کنار هم نگه دارد. در ترکیبات قطبی به علت وجود اختلاف الکترونگاتیوی بین دو اتم، دو بار جزئی مثبت و منفی در دو سر مولکول حاصل می شود و این نیروی دوقطبی، مولکولها را کنار هم نگه می دارد. برای توجیه حالت مایع و جامد مواد غیرقطبی مانند برم و ید نیز، نیروی جاذبه دیگری باید وجود داشته باشد.
چون نقاط ذوب و جوش مواد غیرقطبی با افزایش جرم مولکولی بالا می رود، نتیجه می گیریم که مقدار این نیرو نیز با جرم و اندازه مولکول زیاد می شود. این واقعیت که فراریت مولکولهای قطبی مانند مولکولهای غیرقطبی با افزایش وزن مولکولی کم می شود، نشان می دهد که این نوع نیروی بین مولکولی باید برای همه مواد مولکولی متداول باشد.
منشأ و دلیل به وجود آمدن این نیروی بین مولکولی در سال ۱۹۳۰، توسط "فرتیز لاندن" توضیح داده شد. این نیرو همانند سایر نیروهای بین مولکولی ( دوقطبی - دوقطبی و پیوند هیدروژنی ) ماهیت الکتریکی دارد. اما برخلاف آنها که از قطبیت دائم مولکولها به وجود می آیند، نیروی لاندن ( یا پراکندگی ) از جدایی بار موقتی و لحظه ای در درون یک مولکول حاصل می شود.
منشأ ایجاد این نیروها، حرکت الکترونها می باشد. الکترونها در مولکولهای غیرقطبی مانند H2 به طور متوسط به هر اندازه که به یک هسته نزدیک باشند، به همان اندازه به هسته دیگر نزدیکند. اما در یک لحظه ابر الکترونی می تواند در یک انتهای مولکول متمرکز شود و در لحظه بعد این ابر الکترونی در انتهای دیگر مولکول باشد.
چگالی لحظه ای الکترونها در یک طرف مولکول و قسمت دیگر آن یک دوقطبی موقت در مولکول H2 به وجود می آورد. این موضوع به نوبه خود یک دوقطبی مشابه در مولکول مجاور القا می کند. این دوقطبی های موقت که هر دو در یک مسیر جهت یابی شده اند، نیروی جاذبه ای میان مولکولها ایجاد می کنند که به نیروی پراکندگی یا لاندن معروف است.
قدرت نیروهای لاندن به این بستگی دارد که وقتی یک دوقطبی موقت در مجاورت یک مولکول برقرار می شود، با چه سهولتی می تواند توزیع الکترونی آن مولکول را قطبیده کند. سهولت قطبی شدن در درجه اول به اندازه مولکول بستگی دارد. دوقطبی شدن مولکولهای بزرگ که الکترونها دورتر از هسته می باشند، آسانتر از مولکولهای کوچک که الکترونها به هسته نزدیک هستند صورت می گیرد. با افزایش اندازه مولکول و وزن مولکول بر قدرت نیروهای لاندن افزوده می شود.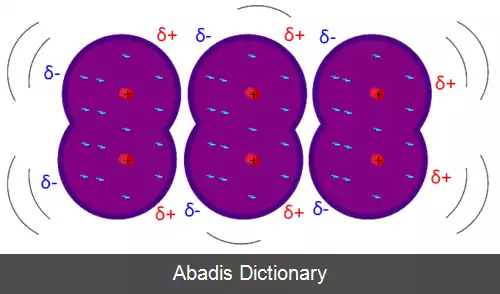
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفبرای اینکه ترکیبی به صورت جامد یا مایع باشد. باید نیروهایی، مولکولهای آن ترکیب را کنار هم نگه دارد. در ترکیبات قطبی به علت وجود اختلاف الکترونگاتیوی بین دو اتم، دو بار جزئی مثبت و منفی در دو سر مولکول حاصل می شود و این نیروی دوقطبی، مولکولها را کنار هم نگه می دارد. برای توجیه حالت مایع و جامد مواد غیرقطبی مانند برم و ید نیز، نیروی جاذبه دیگری باید وجود داشته باشد.
چون نقاط ذوب و جوش مواد غیرقطبی با افزایش جرم مولکولی بالا می رود، نتیجه می گیریم که مقدار این نیرو نیز با جرم و اندازه مولکول زیاد می شود. این واقعیت که فراریت مولکولهای قطبی مانند مولکولهای غیرقطبی با افزایش وزن مولکولی کم می شود، نشان می دهد که این نوع نیروی بین مولکولی باید برای همه مواد مولکولی متداول باشد.
منشأ و دلیل به وجود آمدن این نیروی بین مولکولی در سال ۱۹۳۰، توسط "فرتیز لاندن" توضیح داده شد. این نیرو همانند سایر نیروهای بین مولکولی ( دوقطبی - دوقطبی و پیوند هیدروژنی ) ماهیت الکتریکی دارد. اما برخلاف آنها که از قطبیت دائم مولکولها به وجود می آیند، نیروی لاندن ( یا پراکندگی ) از جدایی بار موقتی و لحظه ای در درون یک مولکول حاصل می شود.
منشأ ایجاد این نیروها، حرکت الکترونها می باشد. الکترونها در مولکولهای غیرقطبی مانند H2 به طور متوسط به هر اندازه که به یک هسته نزدیک باشند، به همان اندازه به هسته دیگر نزدیکند. اما در یک لحظه ابر الکترونی می تواند در یک انتهای مولکول متمرکز شود و در لحظه بعد این ابر الکترونی در انتهای دیگر مولکول باشد.
چگالی لحظه ای الکترونها در یک طرف مولکول و قسمت دیگر آن یک دوقطبی موقت در مولکول H2 به وجود می آورد. این موضوع به نوبه خود یک دوقطبی مشابه در مولکول مجاور القا می کند. این دوقطبی های موقت که هر دو در یک مسیر جهت یابی شده اند، نیروی جاذبه ای میان مولکولها ایجاد می کنند که به نیروی پراکندگی یا لاندن معروف است.
قدرت نیروهای لاندن به این بستگی دارد که وقتی یک دوقطبی موقت در مجاورت یک مولکول برقرار می شود، با چه سهولتی می تواند توزیع الکترونی آن مولکول را قطبیده کند. سهولت قطبی شدن در درجه اول به اندازه مولکول بستگی دارد. دوقطبی شدن مولکولهای بزرگ که الکترونها دورتر از هسته می باشند، آسانتر از مولکولهای کوچک که الکترونها به هسته نزدیک هستند صورت می گیرد. با افزایش اندازه مولکول و وزن مولکول بر قدرت نیروهای لاندن افزوده می شود.

wiki: نیروی پراکندگی لاندن
