نیتروبنزن ( به انگلیسی: Nitrobenzene ) با فرمول شیمیایی C۶H۵NO۲ یک ترکیب شیمیایی با شناسه پاب کم ۷۴۱۶ است. که جرم مولی آن ۱۲۳٫۰۶ g/mol است. شکل ظاهری این ترکیب، مایع مایل به زرد است و بویی شبیه بوی بادام دارد. پس از انجماد به شکل بلورهایی به رنگ زرد - سبز در می آید. نیتروبنزن در مقیاس کلان به عنوان پیشماده ای برای تهیه آنیلین، از بنزن به دست می آید. در آزمایشگاه از آن به عنوان حلال، به ویژه برای واکنشگرهای الکتروفیل، استفاده می شود.
نیتروبنزن را به عنوان پیش ماده ای برای ساخت آنیلین، از نیتراسیون بنزن با مخلوطی از سولفوریک اسید غلیظ و نیتریک اسید، که گاهی اوقات «اسید مختلط» نامیده می شود، تهیه می کنند. تهیه نیتروبنزن یکی از خطرناک ترین فرایندها در صنایع شیمیایی است چرا که واکنش آن بسیار گرمازا است ( ΔH = −117 kJ/mol ) . [ ۴]
در سال ۱۹۸۵ ظرفیت جهانی تولید نیتروبنزن حدود ۱٬۷۰۰٬۰۰۰ تن بود. [ ۴]
مکانیسم نیتراسیون
واکنش نیتراسیون شامل ایجاد یون نیترونیوم ( ) ، همراه با واکنش جانشینی الکتروفیلی آروماتیک بنزن می باشد. یون نیترونیوم از آبگیری نیتریک اسید توسط یک عامل آبگیر اسیدی که معمولاً سولفوریک اسید غلیظ است، تولید می شود:
HNO 3 + H + ↽ − − ⇀ NO 2 + + H 2 O موارد استفاده تقریباً ۹۵٪ نیتروبنزن برای تهیه آنیلین که پیش ماده ای در ساخت مواد شیمیایی مورد استفاده در لاستیک، آفت کش ها، رنگ ها، مواد منفجره و مواد دارویی است، مصرف می شود. [ ۴]
نیتروبنزن به عنوان ماده ای برای کاهش بوهای نامطبوع در پولیش کفپوش و کفش، مصنوعات چرمی، حلال رنگ ها و مواد دیگر استفاده می شود. نیتروبنزن تقطیرمجدد شده را به عنوان ماده معطر ارزان قیمت در ساخت صابون استفاده می کنند. البته این ماده با مواد با سمیت کمتر جایگزین شده است. [ ۵] بازار تجاری ویژه نیتروبنزن در ساخت استامینوفن است ( مانسویل 1991 ) . [ ۶] همچنین نیتروبنزن به علت بالا بودن غیرعادی ثابت کِر آن، در سلول کر ( به انگلیسی: Kerr cell ) استفاده می شود. مدارک نشان می دهند که نیتروبنزن می تواند به عنوان محرک رشد/گلدهی گیاهان در کشاورزی استفاده شود. [ ۷]
نیتروبنزن، علاوه بر تبدیل به آنیلین، نیتروبنزن به طور انتخابی به مشتقات مشابه دیگری مانند آزوبنزن، [ ۸] آزوکسی بنزن، [ ۹] نیتروزوبنزن، [ ۱۰] هیدرازوبنزن[ ۱۱] و فنیل هیدروکسیل آمین[ ۱۲] کاهش می یابد. همچنین نیتروبنزن به عنوان اکسیدکننده ملایم در واکنش هایی مانند سنتز کینولین اسکراپ استفاده می شود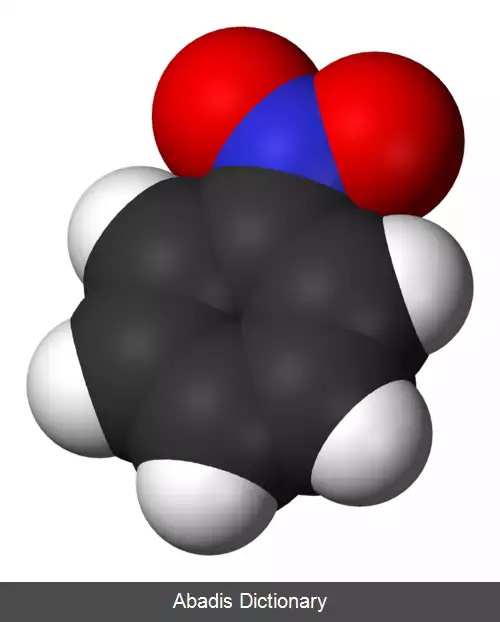

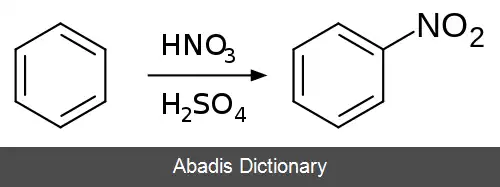
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفنیتروبنزن را به عنوان پیش ماده ای برای ساخت آنیلین، از نیتراسیون بنزن با مخلوطی از سولفوریک اسید غلیظ و نیتریک اسید، که گاهی اوقات «اسید مختلط» نامیده می شود، تهیه می کنند. تهیه نیتروبنزن یکی از خطرناک ترین فرایندها در صنایع شیمیایی است چرا که واکنش آن بسیار گرمازا است ( ΔH = −117 kJ/mol ) . [ ۴]
در سال ۱۹۸۵ ظرفیت جهانی تولید نیتروبنزن حدود ۱٬۷۰۰٬۰۰۰ تن بود. [ ۴]
مکانیسم نیتراسیون
واکنش نیتراسیون شامل ایجاد یون نیترونیوم ( ) ، همراه با واکنش جانشینی الکتروفیلی آروماتیک بنزن می باشد. یون نیترونیوم از آبگیری نیتریک اسید توسط یک عامل آبگیر اسیدی که معمولاً سولفوریک اسید غلیظ است، تولید می شود:
HNO 3 + H + ↽ − − ⇀ NO 2 + + H 2 O موارد استفاده تقریباً ۹۵٪ نیتروبنزن برای تهیه آنیلین که پیش ماده ای در ساخت مواد شیمیایی مورد استفاده در لاستیک، آفت کش ها، رنگ ها، مواد منفجره و مواد دارویی است، مصرف می شود. [ ۴]
نیتروبنزن به عنوان ماده ای برای کاهش بوهای نامطبوع در پولیش کفپوش و کفش، مصنوعات چرمی، حلال رنگ ها و مواد دیگر استفاده می شود. نیتروبنزن تقطیرمجدد شده را به عنوان ماده معطر ارزان قیمت در ساخت صابون استفاده می کنند. البته این ماده با مواد با سمیت کمتر جایگزین شده است. [ ۵] بازار تجاری ویژه نیتروبنزن در ساخت استامینوفن است ( مانسویل 1991 ) . [ ۶] همچنین نیتروبنزن به علت بالا بودن غیرعادی ثابت کِر آن، در سلول کر ( به انگلیسی: Kerr cell ) استفاده می شود. مدارک نشان می دهند که نیتروبنزن می تواند به عنوان محرک رشد/گلدهی گیاهان در کشاورزی استفاده شود. [ ۷]
نیتروبنزن، علاوه بر تبدیل به آنیلین، نیتروبنزن به طور انتخابی به مشتقات مشابه دیگری مانند آزوبنزن، [ ۸] آزوکسی بنزن، [ ۹] نیتروزوبنزن، [ ۱۰] هیدرازوبنزن[ ۱۱] و فنیل هیدروکسیل آمین[ ۱۲] کاهش می یابد. همچنین نیتروبنزن به عنوان اکسیدکننده ملایم در واکنش هایی مانند سنتز کینولین اسکراپ استفاده می شود



wiki: نیتروبنزن
