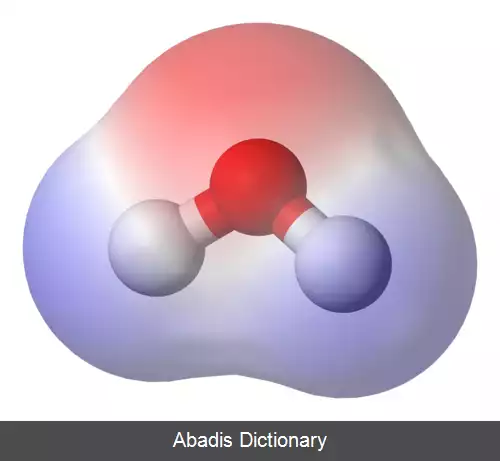
قطبیت شیمیایی ( به انگلیسی: Chemical polarity ) مفهومیست در علم شیمی که بر اساس آن مولکول ها از دیدگاه بار الکتریکی به دو دسته قطبی و غیر قطبی تقسیم بندی می شوند. در مولکول های قطبی مانند آب، نسبت پراکنش الکترون ها در اطراف مولکول نامتوازن نظر بار الکتریکی خنثی است. هیدروکربن ها نمونه مهمی از این نوع مواد هستند.
قطبیت در مولکول ها:
الف ) مولکول دو اتمی:
۱ ) جور هسته: پیوند ناقطبی، مولکول های ناقطبی
مثال:
Cl - Cl
O=O
H - H
۲ ) ناجور هسته: پیوند قطبی، مولکول قطبی
H - I
H - Cl
N=O
ب ) مولکول چند اتمی:
۱ ) قطبی: اتم مرکزی حداقل یکی از شرایط زیر را دارا باشد:
یک ) اتم جانبی متفاوت
دو ) اتم مرکزی دارای جفت ناپیوندی
CHCl3
NH3
H2O
H2S
CH2O
۲ ) ناقطبی:
اتم مرکزی دارای هیچ یک از شرایط ذکر شده در بالا نباشد.
O=C=O CO2
CH4
CCl4
CS2
قطبیت شیمیائی یکی از سه ویژگی اصلی پیوندهای شیمیایی است؛ دو ویژگی دیگر استحکام پیوند ( به انگلیسی: Bond strength ) و طول پیوند ( به انگلیسی: ( Bond length ) هستند[ ۱]
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفقطبیت در مولکول ها:
الف ) مولکول دو اتمی:
۱ ) جور هسته: پیوند ناقطبی، مولکول های ناقطبی
مثال:
Cl - Cl
O=O
H - H
۲ ) ناجور هسته: پیوند قطبی، مولکول قطبی
H - I
H - Cl
N=O
ب ) مولکول چند اتمی:
۱ ) قطبی: اتم مرکزی حداقل یکی از شرایط زیر را دارا باشد:
یک ) اتم جانبی متفاوت
دو ) اتم مرکزی دارای جفت ناپیوندی
CHCl3
NH3
H2O
H2S
CH2O
۲ ) ناقطبی:
اتم مرکزی دارای هیچ یک از شرایط ذکر شده در بالا نباشد.
O=C=O CO2
CH4
CCl4
CS2
قطبیت شیمیائی یکی از سه ویژگی اصلی پیوندهای شیمیایی است؛ دو ویژگی دیگر استحکام پیوند ( به انگلیسی: Bond strength ) و طول پیوند ( به انگلیسی: ( Bond length ) هستند[ ۱]



wiki: قطبیت شیمیایی
