قانون اول ترمودینامیک که به عنوان قانون بقای کار و انرژی نیز شناخته می شود. طبق این قانون برای سیستمی که یک چرخه را طی می کند انتگرال سیکلی گرما با انتگرال سیکلی کار برابر می باشد. حالت تعادل ماکروسکوپی یک سیستم با کمیتی به نام انرژی درونی ( U ) بیان می شود. [ ۱] انرژی درونی دارای خاصیتی است که برای یک سیستم منزوی ( ایزوله ) داریم:
اگر به سیستم اجازهٔ برهم کنش با محیط داده شود، سیستم از حالت ماکروسکوپی اولیهٔ خود به حالت ماکروسکوپی دیگری منتقل می شود که تغییر انرژی درونی را برای این تحول ( فرایند ) می توان به شکل زیر نشان داد:
که در این فرمول W، کار ماکروسکوپی انجام شده توسط سیستم در برابر نیروی خارجی و Q مقدار گرمای جذب شده توسط سیستم در طی این فرایند است. بهتر است به صورت Q=U+W برای محاسبات استفاده شود و برای علامت گذاری، گرمای ورودی به سیستم و کار خروجی از سیستم را مثبت و در غیر اینصورت منفی لحاظ کنیم. [ ۲]
چون در شیمی و فیزیک سیستم مورد توجه است، گرما و کاری که به سیستم داده می شود مورد نظر ماست و انرژی درونی را Q+W در نظر می گیریم. ( سیستم را بسته، در حالت سکون و در غیاب میدان ها در نظر می گیریم )
که در آن
در واقع تعریف قانون اول چنین است: اگر به سیستمی گرما داده شود یا از آن گرما گرفته شود، انرژی درونی سیستم تغییر خواهد نمود که حاصل آن کار انجام شده توسط سیستم یا کار مورد نیاز سیستم برای تغییر انرژی درونی خواهد بود.
تاریخچه
فرایند توسعه قانون اول ترمودینامیک از طریق آزمایش از نوع سعی و خطا در طی یک دوره در حدود نیم قرن بود. اولین اظهارات کامل از قانون در سال ۱۸۵۰ توسط رودلف کلاوزیوس و ویلیام رانکین عنوان شد. ادعاهای رانکین شاید کاملاً به واضح بودن و مشخص بودن بیانیه کلاوزیوس نبود. ( ۱ ) یکی از جنبه های اصلی مبارزه برای مقابله با نظریه کالری بود که قبلاً ارائه شده بود به عنوان " گرما". ژرمن هس در سال ۱۸۴۰ یک قانون حفاظت به اصطلاح 'گرمای واکنش' برای واکنش های شیمیایی اعلام کرد. ( ۲ ) قانون او بعدها به عنوان یک نتیجه از قانون اول ترمودینامیک به رسمیت شناخته شد، اما بیانیه هس را به صراحت با رابطه بین مبادلات انرژی توسط گرما و کار مرتبط نبود. با توجه به Truesdell ( 1980 ) ، ژولیوس رابرت فون مایر در سال ۱۸۴۱ بیانیه ای ساخت که بدان معنی است که "در یک فرایند در فشار ثابت، حرارت مورد استفاده برای تولید انبساط که عموماً قابیل تبدیل با کار است"، اما این بیان کلی از قانون اول نبود.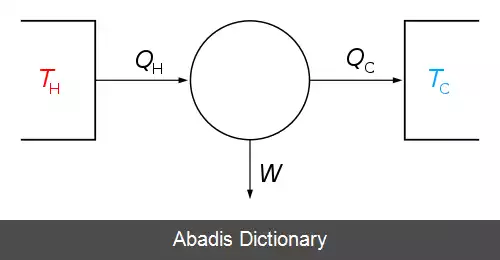
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفاگر به سیستم اجازهٔ برهم کنش با محیط داده شود، سیستم از حالت ماکروسکوپی اولیهٔ خود به حالت ماکروسکوپی دیگری منتقل می شود که تغییر انرژی درونی را برای این تحول ( فرایند ) می توان به شکل زیر نشان داد:
که در این فرمول W، کار ماکروسکوپی انجام شده توسط سیستم در برابر نیروی خارجی و Q مقدار گرمای جذب شده توسط سیستم در طی این فرایند است. بهتر است به صورت Q=U+W برای محاسبات استفاده شود و برای علامت گذاری، گرمای ورودی به سیستم و کار خروجی از سیستم را مثبت و در غیر اینصورت منفی لحاظ کنیم. [ ۲]
چون در شیمی و فیزیک سیستم مورد توجه است، گرما و کاری که به سیستم داده می شود مورد نظر ماست و انرژی درونی را Q+W در نظر می گیریم. ( سیستم را بسته، در حالت سکون و در غیاب میدان ها در نظر می گیریم )
که در آن
در واقع تعریف قانون اول چنین است: اگر به سیستمی گرما داده شود یا از آن گرما گرفته شود، انرژی درونی سیستم تغییر خواهد نمود که حاصل آن کار انجام شده توسط سیستم یا کار مورد نیاز سیستم برای تغییر انرژی درونی خواهد بود.
تاریخچه
فرایند توسعه قانون اول ترمودینامیک از طریق آزمایش از نوع سعی و خطا در طی یک دوره در حدود نیم قرن بود. اولین اظهارات کامل از قانون در سال ۱۸۵۰ توسط رودلف کلاوزیوس و ویلیام رانکین عنوان شد. ادعاهای رانکین شاید کاملاً به واضح بودن و مشخص بودن بیانیه کلاوزیوس نبود. ( ۱ ) یکی از جنبه های اصلی مبارزه برای مقابله با نظریه کالری بود که قبلاً ارائه شده بود به عنوان " گرما". ژرمن هس در سال ۱۸۴۰ یک قانون حفاظت به اصطلاح 'گرمای واکنش' برای واکنش های شیمیایی اعلام کرد. ( ۲ ) قانون او بعدها به عنوان یک نتیجه از قانون اول ترمودینامیک به رسمیت شناخته شد، اما بیانیه هس را به صراحت با رابطه بین مبادلات انرژی توسط گرما و کار مرتبط نبود. با توجه به Truesdell ( 1980 ) ، ژولیوس رابرت فون مایر در سال ۱۸۴۱ بیانیه ای ساخت که بدان معنی است که "در یک فرایند در فشار ثابت، حرارت مورد استفاده برای تولید انبساط که عموماً قابیل تبدیل با کار است"، اما این بیان کلی از قانون اول نبود.

wiki: قانون اول ترمودینامیک
