سدیم دی کرومات ( به انگلیسی: Sodium dichromate ) با فرمول شیمیایی Na۲Cr۲O۷ یک ترکیب غیرآلی است که جرم مولی آن ۲۶۱٫۹۷ g/mol می باشد. تقریباً تمام سنگ معدن کروم با تبدیل آن به سدیم دی کرومات پالایش می شود و تمام ترکیبات و مواد بر پایه کروم از این نمک تهیه می شود. [ ۱] از لحاظ واکنش پذیری و ظاهر، سدیم دی کرومات و پتاسیم دی کرومات بسیار شبیه به هم هستند. همچنین، انحلال پذیری نمک سدیم در آب حدود ۲۰ بار بیشتر از نمک پتاسیم ( ۴۹ گرم در لیتر در ۰ درجه سلسیوس ) است و وزن معادل آن نیز پایین تر است که در بعضی مواقع مطلوب است.
سدیم دی کرومات در مقیاس وسیع از سنگ های حاوی کروم ( III ) اکسید تولید می شود. سنگ معدنی آن با یک باز، معمولا سدیم کربنات، در دمای حدود ۱۰۰۰ درجه سلسیوس در حضور هوا ( منبع اکسیژن ) ذوب می شود:
2Cr2O3 + 4Na2CO3 + 3O2 ⟶ 4Na2CrO4 + 4CO2
این مرحله کروم را قابل حل می کند و اجازه می دهد که کروم به داخل آب گرم استخراج شود. در این مرحله، دیگر اجزای سنگ معدن مانند ترکیبات آلومینیوم و آهن، مقدار کمی قابل حل هستند. اسیدی کردن محلول حاصل شده به وسیله اسید سولفوریک یا کربن دی اکسید باعث تولید دی کرومات می شود:
2Na2CrO4 + 2CO2 + H2O ⟶Na2Cr2O7 + 2NaHCO3
2Na2CrO4 +H2SO4 ⟶ Na2Cr2O7 + Na2SO4 + H2O
دی کرومات به صورت دی هیدرات توسط فرایند کریستالیزاسیون جدا شده است. به این ترتیب سالانه میلیون ها کیلوگرم دی کرومات سدیم تولید می شود. از آنجا که کروم ( VI ) سمی است، به خصوص به صورت گرد و غبار، به کارخانه های آن قوانین سختگیرانه ای اعمال می شود. به عنوان مثال، پساب چنین پالایشگاه هایی با عوامل کاهش دهنده برای بازگشت هر کروم ( VI ) به کروم ( III ) که خطر کمتری برای محیط زیست دارد، تصفیه می شوند. تعداد زیادی از هیدراتهای این نمک شناخته شده است، از جمله هیدرات کمتر از ۱۹٫۵ درجه سلسیوس ( CAS # 13517 - 17 - 4 ) و همچنین هگزا، تترا و دی هیدرات ها. در دمای بیش از ۶۲ درجه سلسیوس، این نمکها به صورت خود به خودی آب از دست می دهند تا مواد بی آب را به دست آورند. این ماده در دمای حدود ۳۰ تا ۳۵ درجه سلسیوس بلورین می شود.
سدیم دی کرومات نیز مثل تمام ترکیبات کروم شش ظرفیتی خطرناک است. همچنین یک عامل سرطان زا نیز شناخته می شود. [ ۲]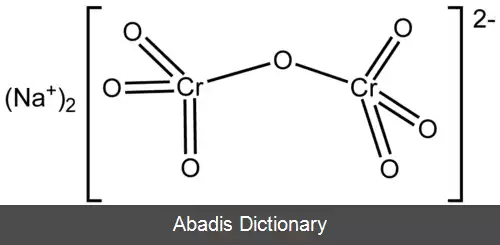

این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفسدیم دی کرومات در مقیاس وسیع از سنگ های حاوی کروم ( III ) اکسید تولید می شود. سنگ معدنی آن با یک باز، معمولا سدیم کربنات، در دمای حدود ۱۰۰۰ درجه سلسیوس در حضور هوا ( منبع اکسیژن ) ذوب می شود:
2Cr2O3 + 4Na2CO3 + 3O2 ⟶ 4Na2CrO4 + 4CO2
این مرحله کروم را قابل حل می کند و اجازه می دهد که کروم به داخل آب گرم استخراج شود. در این مرحله، دیگر اجزای سنگ معدن مانند ترکیبات آلومینیوم و آهن، مقدار کمی قابل حل هستند. اسیدی کردن محلول حاصل شده به وسیله اسید سولفوریک یا کربن دی اکسید باعث تولید دی کرومات می شود:
2Na2CrO4 + 2CO2 + H2O ⟶Na2Cr2O7 + 2NaHCO3
2Na2CrO4 +H2SO4 ⟶ Na2Cr2O7 + Na2SO4 + H2O
دی کرومات به صورت دی هیدرات توسط فرایند کریستالیزاسیون جدا شده است. به این ترتیب سالانه میلیون ها کیلوگرم دی کرومات سدیم تولید می شود. از آنجا که کروم ( VI ) سمی است، به خصوص به صورت گرد و غبار، به کارخانه های آن قوانین سختگیرانه ای اعمال می شود. به عنوان مثال، پساب چنین پالایشگاه هایی با عوامل کاهش دهنده برای بازگشت هر کروم ( VI ) به کروم ( III ) که خطر کمتری برای محیط زیست دارد، تصفیه می شوند. تعداد زیادی از هیدراتهای این نمک شناخته شده است، از جمله هیدرات کمتر از ۱۹٫۵ درجه سلسیوس ( CAS # 13517 - 17 - 4 ) و همچنین هگزا، تترا و دی هیدرات ها. در دمای بیش از ۶۲ درجه سلسیوس، این نمکها به صورت خود به خودی آب از دست می دهند تا مواد بی آب را به دست آورند. این ماده در دمای حدود ۳۰ تا ۳۵ درجه سلسیوس بلورین می شود.
سدیم دی کرومات نیز مثل تمام ترکیبات کروم شش ظرفیتی خطرناک است. همچنین یک عامل سرطان زا نیز شناخته می شود. [ ۲]


wiki: سدیم دی کرومات
