آنزیم زانتین اکسیداز ( به انگلیسی: Xanthine oxidase ) که آن را به طور مخفف با XO و در بعضی مواقع با XAO نشان می دهند شکلی از زانتین اکسیدو رداکتاز می باشد.
این پروتئین بزرگ دارای وزن مولکولی 160KDa می باشد. نقطه ایزوالکتریک زانتین اکسیداز ۴، pH optimum آن ۷ تا ۵/۷ و دمای اپتیمم ۵۵ درجه سانتی گراد می باشد
اتم های مولیبیدن، کوفاکتورهای مولیدوپترین را تشکیل می دهند و بخش فعال یا همان Active site آنزیم هستند. اتم های آهن بخشی از کلاستر ferredoxine iron - sulfur هستند و در واکنش های انتقال الکترون دخالت دارند.
همانگونه که در ساختار کریستالی مشاهده می شود در آن هر دو شکل آلفا و بتا وجود دارد.
واکنش های شیمیایی کاتالیز شده توسط زانتین اکسیداز به شرح ذیل می باشد:
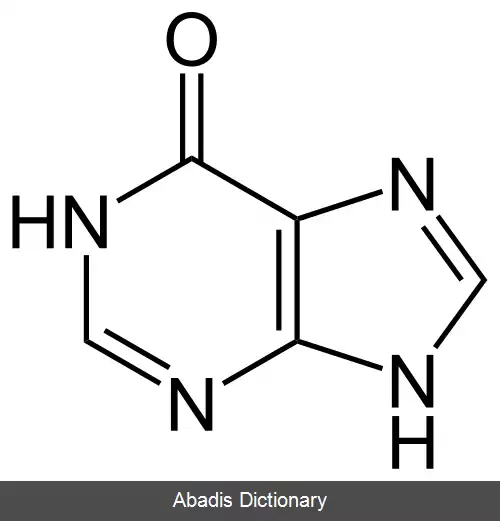
Hypoxanthine + H2O + O2 ↔ xanthine + H2O2
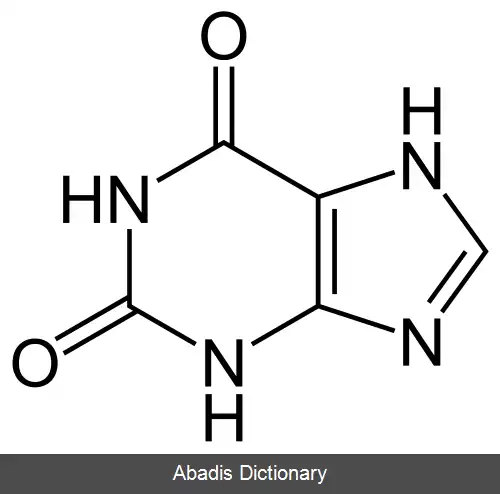
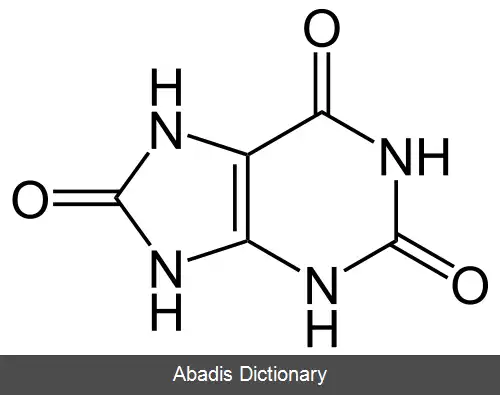
Xanthine + H2O + O2 ↔ uric acid + H2O2
این کاتالیزور هیپوزانتین را به زانتین اکسایش می دهد و مقدار اضافی آن زانتین را به اوریک اسید اکسایش می دهد؛ بنابراین هیپوزانتین به عنوان سوبسترا در مرحله اول می باشد اما سوبسترای اصلی واکنش زانتین است.
افزایش اسید اوریک در خون می تواند موجب بیماری نقرس شود. این بیماری که به آن بیماری پولدارها می گویند به دلیل مصرف زیاد گوشت قرمز ایجاد می شود و درد شدیدی در ناحیه مفصل انگشت شصت پا به همراه دارد.
در ساختار اکتیو سایت زانیتن اکسیداز، گلوتامات ۱۲۶۱ و ۸۰۲ و همچنین آرژنین ۸۸۰ و تریونین ۱۰۱۰ وجود دارد.
اکتیو سایت زانتین اکسیداز از چهار بخش اصلی: یک مرکز مولیبیدن، یک جفت کلاستر 2Fe - 2s و یک FAD تشکیل شده است.
برخی داروها از جمله آلوپورینول مهارکننده این آنزیم هستند.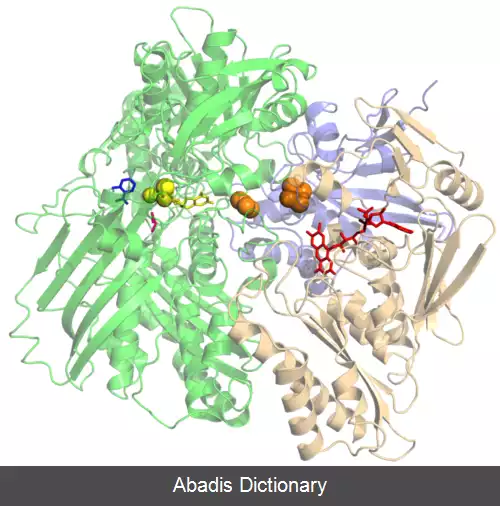
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفاین پروتئین بزرگ دارای وزن مولکولی 160KDa می باشد. نقطه ایزوالکتریک زانتین اکسیداز ۴، pH optimum آن ۷ تا ۵/۷ و دمای اپتیمم ۵۵ درجه سانتی گراد می باشد
اتم های مولیبیدن، کوفاکتورهای مولیدوپترین را تشکیل می دهند و بخش فعال یا همان Active site آنزیم هستند. اتم های آهن بخشی از کلاستر ferredoxine iron - sulfur هستند و در واکنش های انتقال الکترون دخالت دارند.
همانگونه که در ساختار کریستالی مشاهده می شود در آن هر دو شکل آلفا و بتا وجود دارد.
واکنش های شیمیایی کاتالیز شده توسط زانتین اکسیداز به شرح ذیل می باشد:
Hypoxanthine + H2O + O2 ↔ xanthine + H2O2
Xanthine + H2O + O2 ↔ uric acid + H2O2
این کاتالیزور هیپوزانتین را به زانتین اکسایش می دهد و مقدار اضافی آن زانتین را به اوریک اسید اکسایش می دهد؛ بنابراین هیپوزانتین به عنوان سوبسترا در مرحله اول می باشد اما سوبسترای اصلی واکنش زانتین است.
افزایش اسید اوریک در خون می تواند موجب بیماری نقرس شود. این بیماری که به آن بیماری پولدارها می گویند به دلیل مصرف زیاد گوشت قرمز ایجاد می شود و درد شدیدی در ناحیه مفصل انگشت شصت پا به همراه دارد.
در ساختار اکتیو سایت زانیتن اکسیداز، گلوتامات ۱۲۶۱ و ۸۰۲ و همچنین آرژنین ۸۸۰ و تریونین ۱۰۱۰ وجود دارد.
اکتیو سایت زانتین اکسیداز از چهار بخش اصلی: یک مرکز مولیبیدن، یک جفت کلاستر 2Fe - 2s و یک FAD تشکیل شده است.
برخی داروها از جمله آلوپورینول مهارکننده این آنزیم هستند.




wiki: زانتین اکسیداز
