توزیع ماکسول–بولتزمن ( به انگلیسی: Maxwell–Boltzmann distribution ) در فیزیک و به ویژه در مکانیک آماری، تابعی است که توزیع سرعت ذرات را در گاز مشخص می کند. ویژگی گاز ایده آل این است که ذرات گاز در فواصل کوچک به آزادی حرکت می کنند و حتی برخورد با دیگر ذرات دارند، اما برهم کنشی روی یکدیگر ندارند. این توزیع تابعی از دمای سامانه، جرم و سرعت ذرات است. ذره در این جا هم به معنی مولکول و هم به معنی اتم است.
توزیع ماکسول–بولتزمن در گاز ایده آل نزدیک به تعادل ترمودینامیکی با اثرات کوانتمی ناچیز و سرعت غیرنسبیتی صحیح است. هم چنین این توزیع از پایه های نظریه جنبشی است، که خودش خصوصیات بنیادی گازها مانند فشار را به صورت ساده توضیح می دهد. [ ۱] در سرعت های نسبیتی تابع توزیع «ماکسول–جوتنر» استفاده می شود.
توزیع ماکسول–بولتزمن شالوده ی نظریه جنبشی گازها است.
جیمز کلرک ماکسول در سال ۱۸۶۰ این توزیع را به عنوان ابزاری آماری برای توضیح جنبه های گوناگونِ نظریه جنبشی گازها کشف کرده و گسترش داد. سپس لودویگ بولتزمان تحقیقات مهمی بر روی منشا فیزیکی چنین توزیعی را انجام داد.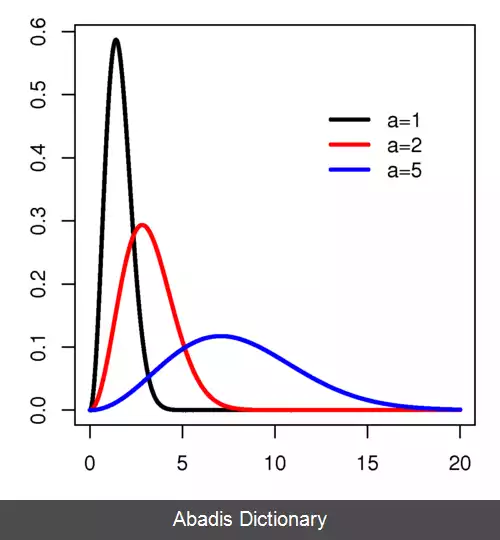
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفتوزیع ماکسول–بولتزمن در گاز ایده آل نزدیک به تعادل ترمودینامیکی با اثرات کوانتمی ناچیز و سرعت غیرنسبیتی صحیح است. هم چنین این توزیع از پایه های نظریه جنبشی است، که خودش خصوصیات بنیادی گازها مانند فشار را به صورت ساده توضیح می دهد. [ ۱] در سرعت های نسبیتی تابع توزیع «ماکسول–جوتنر» استفاده می شود.
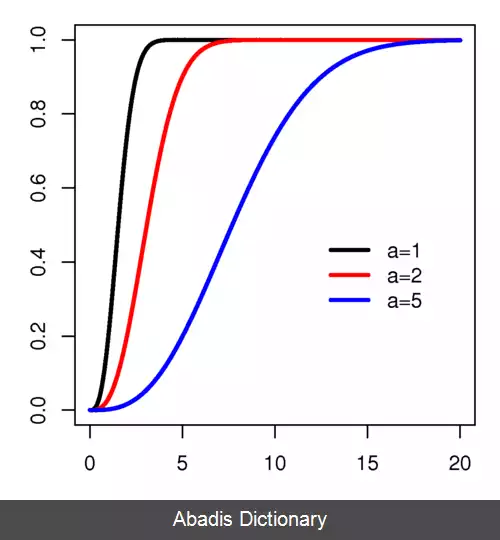
توزیع ماکسول–بولتزمن شالوده ی نظریه جنبشی گازها است.
جیمز کلرک ماکسول در سال ۱۸۶۰ این توزیع را به عنوان ابزاری آماری برای توضیح جنبه های گوناگونِ نظریه جنبشی گازها کشف کرده و گسترش داد. سپس لودویگ بولتزمان تحقیقات مهمی بر روی منشا فیزیکی چنین توزیعی را انجام داد.


wiki: توزیع ماکسول بولتسمان
