تُهی جایی یا جای خالی ( به انگلیسی: Vacancy ) در بلورشناسی یکی از ساده ترین و مهم ترین عیوب نقطه ای است. تهی جایی به عدم وجود اتم یا یون به تعداد متناهی در شبکه بلوری ماده گفته می شود. تمامی جامدات بلوری دارای جاهای خالی هستند در واقع بسیار مشکل است که ماده ای ساخته شود که دارای این عیب نباشد. چنین عیوبی می تواند در مواقع انجماد، تغییر شکل دادن، اشعه دادن با انرژی زیاد یا در درجه حرارت های بالا به وجود بیایند. وجود نقص جای خالی منجر به نزدیک شدن اتم های اطراف جای خالی می شود و نظم اتمی اندکی به هم می ریزد و همچنین باعث افزایش انتروپی ( Entropy ) بلور می گردد.
در یک جسم در حالت تعادل همیشه تعدادی جای خالی وجود دارد که تعداد تعادلی جاهای خالی برای مقدار معینی از ماده وابسته به دما است. در حقیقت در هر دمایی تا دمای ذوب جامد بلوری رابطه ای بین تعداد مکان های خالی و مکان های دارای اتم برقرار است که از رابطه زیر بدست می آید:
N v = N e x p ( − Q v / k B T )
( N = ρ N A / A )
که در آن N v تعداد تعادلی جاهای خالی، N تعداد کل مکان های اتمی، Q v انرژی لازم برای تشکیل جاهای خالی، K B ثابت بولتزمن، T دما برحسب کلوین، ρ چگالی، N A عدد آووگادرو و A جرم اتمی است. همچنین مشاهده شده است که در دمای ذوب بعضی مواد این نسبت ۱:۱۰۰۰ است.
اما در درجه حرارت بالاتر از حدود نقطه ذوب عیوب جای خالی از بین خواهند رفت زیرا در حالت مذاب شبکه کریستالی کاملاً بهم خواهد ریخت و همچنین لزوم حضور جاهای خالی را نیز با استفاده از اصول ترمودینامیک می توان اثبات نمود و تنها این عیوب هستند که در حالت حرارتی به وجود می آیند و بقیه عیوب کریستالی از نظر ترمودینامیکی در تعادل نیست و در اثر عوامل خارجی به وجود می آیند.
نقص جای خالی از عیوبی است که پدیده نفوذ را آسان تر می نماید و کاربردهای ویژه ای در ساخت مواد و آلیاژهایی با ویژگی های خاص و قابل کنترل دارد و سبب بروز تغییراتی در رنگ کریستال می گردد، استفاده صنعتی ای که از این عیوب می گردد در ساخت بلورهای نیم رسانا و نیمه عایق است.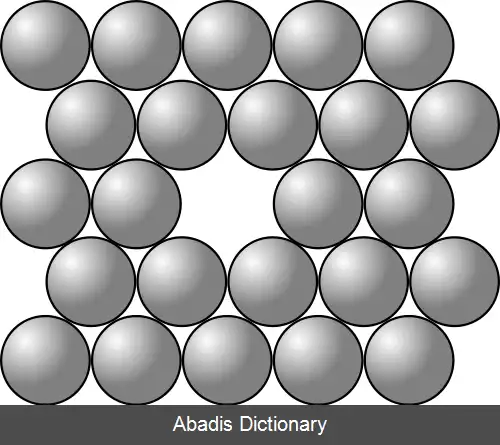
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفدر یک جسم در حالت تعادل همیشه تعدادی جای خالی وجود دارد که تعداد تعادلی جاهای خالی برای مقدار معینی از ماده وابسته به دما است. در حقیقت در هر دمایی تا دمای ذوب جامد بلوری رابطه ای بین تعداد مکان های خالی و مکان های دارای اتم برقرار است که از رابطه زیر بدست می آید:
N v = N e x p ( − Q v / k B T )
( N = ρ N A / A )
که در آن N v تعداد تعادلی جاهای خالی، N تعداد کل مکان های اتمی، Q v انرژی لازم برای تشکیل جاهای خالی، K B ثابت بولتزمن، T دما برحسب کلوین، ρ چگالی، N A عدد آووگادرو و A جرم اتمی است. همچنین مشاهده شده است که در دمای ذوب بعضی مواد این نسبت ۱:۱۰۰۰ است.
اما در درجه حرارت بالاتر از حدود نقطه ذوب عیوب جای خالی از بین خواهند رفت زیرا در حالت مذاب شبکه کریستالی کاملاً بهم خواهد ریخت و همچنین لزوم حضور جاهای خالی را نیز با استفاده از اصول ترمودینامیک می توان اثبات نمود و تنها این عیوب هستند که در حالت حرارتی به وجود می آیند و بقیه عیوب کریستالی از نظر ترمودینامیکی در تعادل نیست و در اثر عوامل خارجی به وجود می آیند.
نقص جای خالی از عیوبی است که پدیده نفوذ را آسان تر می نماید و کاربردهای ویژه ای در ساخت مواد و آلیاژهایی با ویژگی های خاص و قابل کنترل دارد و سبب بروز تغییراتی در رنگ کریستال می گردد، استفاده صنعتی ای که از این عیوب می گردد در ساخت بلورهای نیم رسانا و نیمه عایق است.

wiki: تهی جایی
