بتا - پپتیدها همانند پپتیدهای معمولی، رشته ای از آمینواسیدها هستند با این تفاوت که آمینواسیدهای آن، β - آمینواسید هستند. β - آمینواسیدها آمینواسیدهایی هستند که گروه آمین آن ها به جای اتصال به کربن α، به کربن β متصل است. کربن α، مجاور گروه کربوکسیل و کربن β مجاور کربن α قرار دارد. درنتیجه میان گروه کربونیل و گروه آمین در β - پپتیدها، دو کربن به جای یک کربن قرار گرفته است. همه انواع آمینواسیدهای طبیعی، از نوع آلفا هستند و تنها آمینواسید بتا در طبیعت، β - آلانین است. بنابراین β - پپتیدی به صورت طبیعی وجود ندارد و به طور مصنوعی ساخته می شود. از اهمیت β - پپتیدها می توان به ساخت آنتی بیوتیک های β - پپتیدی اشاره کرد که توسط مهارکننده های آنتی بیوتیک در بدن مهار نمی شوند. [ ۱]
در یک α - آمینو اسید همان طور که در شکل مشاهده می شود، هر دو گروه کربوکسیل ( قرمز ) و آمین ( آبی ) به یک کربن که به کربن آلفا ( α ) معروف است متصل اند. در مقابل، در β - آمینواسیدها گروه آمینی به کربن مجاور کربن آلفا، که به کربن بتا ( β ) معروف است متصل است. همه آمینواسیدهای طبیعی علاوه بر کربن آلفا، کربن بتا هم دارند به جز گلایسین که ساده ترین آمینواسید طبیعت است. درنتیجه β - گلایسین وجود ندارد.
سنتز بتا - پپتیدها می تواند چالش برانگیز باشد چرا که گروه های عاملی مختلفی روی کربن بتای آمینواسیدها قرار دارد و همین طور حفظ پیکربندی در صورت کایرال بودن کربن بتا دشوار است. کربن بتای β - آلانین، کایرال نیست اما اکثر β - آمینواسیدهای غول پیکر این ویژگی را ندارند و این موضوع ساخت آن ها را دشوارتر می کند. با این حال روش های ساخت موثری برای تولید β - آمینواسیدها ارائه شده است که اکثر آن ها مبتنی بر روش سنتز آرنت ایسترت هستند. [ ۲] [ ۳]
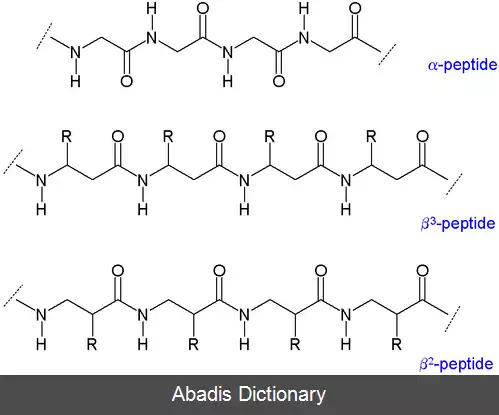
دو ساختار اصلی برای β - پپتیدها وجود دارد: دسته اول پپتیدهایی که گروه های آلی ( که با R نشان داده می شوند ) به کربن β متصل اند. به پپتیدهای این دسته، β3 - پپتید گویند. در دسته دوم، این گروه ها به کربن α متصل اند و آن ها را β2 - پپتید می خوانند. [ ۴]
اسکلت اصلی بتا - پپتیدها نسبت به پپتیدهایی که از آمینواسیدهای آلفا تشکیل شده اند، طولانی تر است. به همین دلیل با توجه به اینکه پپتیدها به طور کلی رشته های بلندی هستند، آرایش فضایی بتا - پپتیدها از پپتیدهای دیگر متفاوت است. استخلافهای متصل به کربن بتا و آلفا، صورتبندی گوچ را در راستای پیوند کربن آلفا و بتا اختیار می کنند. این مساله به دلیل پایداری ترمودینامیکی مولکول انجام می گیرد و باعث ایجاد ساختارهای مارپیچ بیشتر و متفاوت تری نسبت به پپتیدهای آلفا می شود. [ ۵]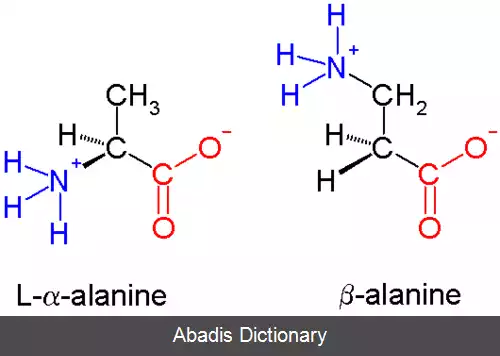
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفدر یک α - آمینو اسید همان طور که در شکل مشاهده می شود، هر دو گروه کربوکسیل ( قرمز ) و آمین ( آبی ) به یک کربن که به کربن آلفا ( α ) معروف است متصل اند. در مقابل، در β - آمینواسیدها گروه آمینی به کربن مجاور کربن آلفا، که به کربن بتا ( β ) معروف است متصل است. همه آمینواسیدهای طبیعی علاوه بر کربن آلفا، کربن بتا هم دارند به جز گلایسین که ساده ترین آمینواسید طبیعت است. درنتیجه β - گلایسین وجود ندارد.
سنتز بتا - پپتیدها می تواند چالش برانگیز باشد چرا که گروه های عاملی مختلفی روی کربن بتای آمینواسیدها قرار دارد و همین طور حفظ پیکربندی در صورت کایرال بودن کربن بتا دشوار است. کربن بتای β - آلانین، کایرال نیست اما اکثر β - آمینواسیدهای غول پیکر این ویژگی را ندارند و این موضوع ساخت آن ها را دشوارتر می کند. با این حال روش های ساخت موثری برای تولید β - آمینواسیدها ارائه شده است که اکثر آن ها مبتنی بر روش سنتز آرنت ایسترت هستند. [ ۲] [ ۳]
دو ساختار اصلی برای β - پپتیدها وجود دارد: دسته اول پپتیدهایی که گروه های آلی ( که با R نشان داده می شوند ) به کربن β متصل اند. به پپتیدهای این دسته، β3 - پپتید گویند. در دسته دوم، این گروه ها به کربن α متصل اند و آن ها را β2 - پپتید می خوانند. [ ۴]
اسکلت اصلی بتا - پپتیدها نسبت به پپتیدهایی که از آمینواسیدهای آلفا تشکیل شده اند، طولانی تر است. به همین دلیل با توجه به اینکه پپتیدها به طور کلی رشته های بلندی هستند، آرایش فضایی بتا - پپتیدها از پپتیدهای دیگر متفاوت است. استخلافهای متصل به کربن بتا و آلفا، صورتبندی گوچ را در راستای پیوند کربن آلفا و بتا اختیار می کنند. این مساله به دلیل پایداری ترمودینامیکی مولکول انجام می گیرد و باعث ایجاد ساختارهای مارپیچ بیشتر و متفاوت تری نسبت به پپتیدهای آلفا می شود. [ ۵]


wiki: بتا پپتید
