باتری آلومینیومی یونی. باتری های آلومینیوم یونی ( به انگلیسی: Aluminium - ion batteries ) دسته ای از باتری های قابل شارژ هستند که در آن یونهای آلومینیوم با جریان یافتن از سمت الکترود منفی باتری یعنی آند، به الکترود مثبت یعنی کاتد، انرژی الکتریکی را تولید می کنند. در هنگام شارژ مجدد، یون های آلومینیوم به الکترود منفی برمی گردند که یون می تواند سه الکترون را مبادله کنند. این بدان معنی است که یک یون Al+3 معادل سه یون Li+1 در کاتدهای معمولی است. همچنین با توجه به آن که از آنجا که شعاع یونی Al+3 و Li+1 نزدیک هستند، تعداد الکترون ها ی بیشتری بوسیله Al+3 می تواند جذب کاتدها شود بدون آن که پودر شوند. در واقع وجود ۳ الکترون در یون Al+3 هم مزیت و هم نقطه ضعف این نوع باتری است. در واقع انتقال ۳ واحد بار توسط یک یون به طور قابل توجهی ظرفیت ذخیره انرژی را افزایش می دهد که نکته مثبتی است اما از طرفی دیگر نیز درهم آمیختگی الکترواستاتیکی ماده میزبان با یک کاتیون سه ظرفیتی، یک واکنش الکتروشیمیایی بسیار قوی است. [ ۱] [ ۲] [ ۳]
باتری های مبتنی بر آلومینیوم قابل شارژ، علاوه بر قابلیت هایی همچون کم هزینه بودن و قابلیت اشتعال پایین، به علت وجود یون های دارای سه الکترون، ظرفیت بالایی نیز دارند. انتظار می رود بی اثر بودن آلومینیوم و سهولت کار با آن در یک محیط عادی، بهبود قابل توجهی در ایمنی برای این نوع باتری ها ایجاد کند. بعلاوه، آلومینیوم به دلیل چگالی بالای خود در مقایسه با لیتیم، پتاسیم، منیزیم، سدیم، کلسیم و روی از ظرفیت حجمی به نسبت بالاتری نیز برخوردار است. این به این معنی است که انرژی ذخیره شده در باتری های آلومینیوم به ازای واحد حجم، بیشتر از انرژی باتری های فلزی دیگر است بنابراین انتظار می رود که اندازه باتری های آلومینیوم کوچکتر باشد. همچنین باتری های آلومینیوم یونی تعداد سیکل های شارژ بیشتری دارند؛ بنابراین، باتری های آلومینیوم یونی توانایی جایگزینی باتری های لیتیوم یون را دارند.
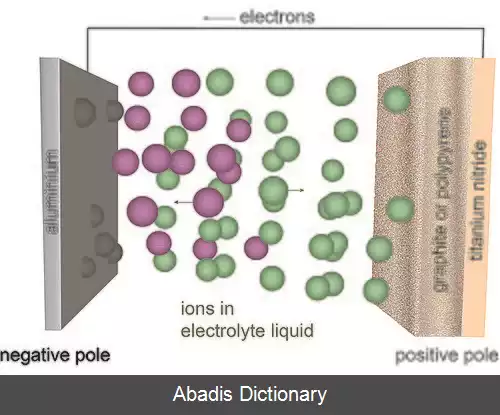
همانند سایر باتری ها، ساختار اصلی باتری های آلومینیوم یونی نیز تشکیل شده از دو الکترود است که بوسیله یک الکترولیت بهم دیگر متصل می شون. در واقع الکترولیت یک ماده رسانایی یونی ( و نه الکتریکی ) است که واسطه ای برای جریان یافتن حامل های بار است.
بر خلاف باتری های یون لیتیوم، جایی که یون متحرک Li+1 است، آلومینیوم در اکثر الکترولیت ها با کلرید واکنش می دهد و یک حامل بار متحرک آنیونی، معمولاً AlCl۴–1 یا Al2Cl7 - 1 تولید می کند. [ ۴] میزان انرژی یا توانی که باتری می تواند آزاد کند به عواملی از جمله ولتاژ، ظرفیت سلول و ترکیب شیمیایی سلول باتری بستگی دارد. یک باتری می تواند میزان انرژی خروجی را بوسیله موارد زیر به حداکثر برساند:[ ۵]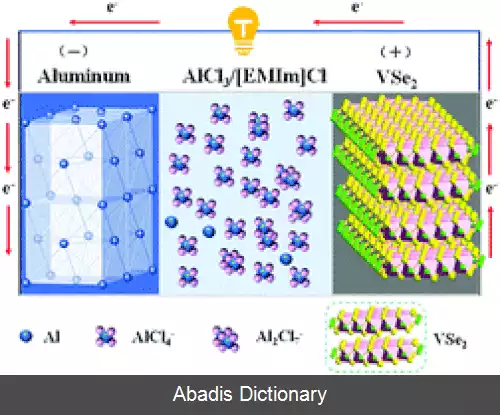
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفباتری های مبتنی بر آلومینیوم قابل شارژ، علاوه بر قابلیت هایی همچون کم هزینه بودن و قابلیت اشتعال پایین، به علت وجود یون های دارای سه الکترون، ظرفیت بالایی نیز دارند. انتظار می رود بی اثر بودن آلومینیوم و سهولت کار با آن در یک محیط عادی، بهبود قابل توجهی در ایمنی برای این نوع باتری ها ایجاد کند. بعلاوه، آلومینیوم به دلیل چگالی بالای خود در مقایسه با لیتیم، پتاسیم، منیزیم، سدیم، کلسیم و روی از ظرفیت حجمی به نسبت بالاتری نیز برخوردار است. این به این معنی است که انرژی ذخیره شده در باتری های آلومینیوم به ازای واحد حجم، بیشتر از انرژی باتری های فلزی دیگر است بنابراین انتظار می رود که اندازه باتری های آلومینیوم کوچکتر باشد. همچنین باتری های آلومینیوم یونی تعداد سیکل های شارژ بیشتری دارند؛ بنابراین، باتری های آلومینیوم یونی توانایی جایگزینی باتری های لیتیوم یون را دارند.
همانند سایر باتری ها، ساختار اصلی باتری های آلومینیوم یونی نیز تشکیل شده از دو الکترود است که بوسیله یک الکترولیت بهم دیگر متصل می شون. در واقع الکترولیت یک ماده رسانایی یونی ( و نه الکتریکی ) است که واسطه ای برای جریان یافتن حامل های بار است.
بر خلاف باتری های یون لیتیوم، جایی که یون متحرک Li+1 است، آلومینیوم در اکثر الکترولیت ها با کلرید واکنش می دهد و یک حامل بار متحرک آنیونی، معمولاً AlCl۴–1 یا Al2Cl7 - 1 تولید می کند. [ ۴] میزان انرژی یا توانی که باتری می تواند آزاد کند به عواملی از جمله ولتاژ، ظرفیت سلول و ترکیب شیمیایی سلول باتری بستگی دارد. یک باتری می تواند میزان انرژی خروجی را بوسیله موارد زیر به حداکثر برساند:[ ۵]


wiki: باتری آلومینیومی یونی
