آمونیوم دی کرومات. آمونیوم دی کرومات ( به انگلیسی: Ammonium dichromate ) ، یک ترکیب غیرآلی است که به دلیل استفاده اش در ایجاد آتش فشان های روی میزی گاهی با نام Vesuvian Fire ( معنی Vesuvian: وابسته به کوه آتش فشان Vesuvius؛ آتش فشانی ) نیز شناخته می شود. این ماده در مواد آتش زنه و در دوران نخستین عکاسی به کار رفته است. این ماده در صنایع شیمیایی و مواد اولیه و همچنین لیتوگرافی ، به عنوان منبع نیتروژن خالص در آزمایشگاه و به عنوان کاتالیزور مورد استفاده قرار گرفته است و همچنین به عنوان ماده رنگی برای رنگ آمیزی رنگدانه ها ، در تولید آلیزارین ، آلوم کروم ، برنزه شدن چرم و تصفیه روغن استفاده می شود
فرمول شیمیایی آمونیوم دی کرومات ( NH4 ) 2Cr2O7 است. این ترکیب یک جامد یونی محسوب می شود که حاوی یونهای آمونیوم ( NH4+ ) و دی کرومات ( Cr2O72 - ) است[ ۲] . در ساختار بلوری، پیوندهای هیدروژنی به جهت دهی این یون ها کنار هم کمک می کنند[ ۳] . به دلیل عدد اکسایش کروم که 6+ است، آمونیوم دی کرومات مانند تمام ترکیبات کروم یک ماده سمی و سرطان زا است همچنین ماده تحریک کننده قوی نیز می باشد
این ماده، همانند اکثر ترکیب های یونی، در دمای معمولی جامد است و نقطه ذوب بالایی دارد. آمونیوم دی کرومات به شکل جامد نارنجی رنگ محلول در آب وجود دارد. انحلال آن در آب به دلیل جاذبه های یون - دوقطبی، پیوند هیدروژنی و هم چنین نیروهای دوقطبی - دوقطبی ( به دلیل قطبیت آنیون ) صورت می گیرد.
واکنش کوه آتش فشان، معروف ترین واکنش آمونیوم دی کرومات است که شامل تجزیه شدن مقداری از این ماده در اثر حرارت و انرژی اولیه است. معادله این واکنش گرماده را در زیر می بینید:
محصول های این واکنش، بخار آب، گاز نیتروژن و جامد سبز رنگ کروم ( III ) اکسید است که در آب نیز نامحلول می باشد.
مانند مادهٔ آمونیوم نیترات شناخته شده، آمونیوم دی کرومات هم شامل یک اکسیدکننده ( دی کرومات ) و هم شامل یک کاهنده ( آمونیوم ) می باشد. [ ۴] .
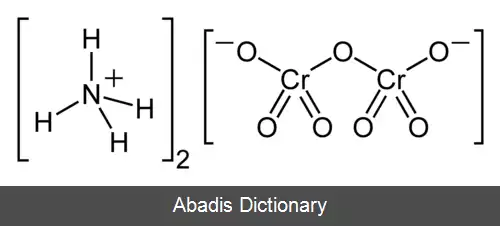
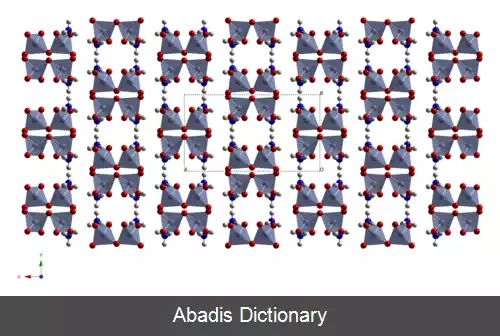
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلففرمول شیمیایی آمونیوم دی کرومات ( NH4 ) 2Cr2O7 است. این ترکیب یک جامد یونی محسوب می شود که حاوی یونهای آمونیوم ( NH4+ ) و دی کرومات ( Cr2O72 - ) است[ ۲] . در ساختار بلوری، پیوندهای هیدروژنی به جهت دهی این یون ها کنار هم کمک می کنند[ ۳] . به دلیل عدد اکسایش کروم که 6+ است، آمونیوم دی کرومات مانند تمام ترکیبات کروم یک ماده سمی و سرطان زا است همچنین ماده تحریک کننده قوی نیز می باشد
این ماده، همانند اکثر ترکیب های یونی، در دمای معمولی جامد است و نقطه ذوب بالایی دارد. آمونیوم دی کرومات به شکل جامد نارنجی رنگ محلول در آب وجود دارد. انحلال آن در آب به دلیل جاذبه های یون - دوقطبی، پیوند هیدروژنی و هم چنین نیروهای دوقطبی - دوقطبی ( به دلیل قطبیت آنیون ) صورت می گیرد.
واکنش کوه آتش فشان، معروف ترین واکنش آمونیوم دی کرومات است که شامل تجزیه شدن مقداری از این ماده در اثر حرارت و انرژی اولیه است. معادله این واکنش گرماده را در زیر می بینید:
محصول های این واکنش، بخار آب، گاز نیتروژن و جامد سبز رنگ کروم ( III ) اکسید است که در آب نیز نامحلول می باشد.
مانند مادهٔ آمونیوم نیترات شناخته شده، آمونیوم دی کرومات هم شامل یک اکسیدکننده ( دی کرومات ) و هم شامل یک کاهنده ( آمونیوم ) می باشد. [ ۴] .



wiki: آمونیوم دی کرومات
