آلومینیم کلرید. آلومینیوم کلرید ( به انگلیسی: Aluminum chloride ) یک ترکیب معدنی است که از دو عنصر آلومنیوم و کلر ساخته شده است. آلومینیم کلرید اگرخالص باشد سفید رنگ وجامد است. این ماده تحت تأثیرگرما تصعید می شود و درمجاورت رطوبت، بخشی ازآلومینیم کلرید بی آب تجزیه و گازهیدروژن کلرید آزاد می شود. این نمک را نخستین باردرسال1825 ارستد تهیه کرد. او گازکلررا از روی مخلوطی ازآلومین و کربن عبورداد و بخارات آلومینیم کلرید تشکیل شده را به مایع تبدیل نمود. امروزه نیزازنظراصولی ازفرایند مشابهی برای تهیه تجارتی آلومینیم کلرید استفاده می گردد.
کلرید آلومینیوم ( AlCl3 ) ، همچنین به عنوان تری کلرید آلومینیوم شناخته می شود ، ترکیباتی را با فرمول AlCl3 ( H2O ) n توصیف می کند ( n = 0یا 6 ) . آنها از اتمهای آلومینیوم و کلر به نسبت 1: 3 تشکیل شده اند و یک فرم نیز حاوی شش آب هیدراتاسیون است. هر دو ماده جامد سفید هستند ، اما نمونه ها اغلب با کلرید آهن ( III ) آلوده می شوند و به آنها رنگ زرد می دهد.
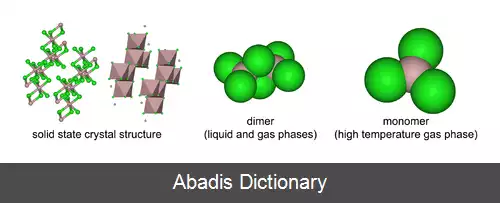
ماده بی آب از نظر تجاری مهم است. دارای نقطه ذوب و جوش کم است. این ماده عمدتاً در تولید فلز آلومینیوم تولید و مصرف می شود ، اما مقادیر زیادی نیز در سایر مناطق صنایع شیمیایی استفاده می شود. [ ۲] این ترکیب اغلب به عنوان اسید لوئیس ذکر می شود. این نمونه ای از یک ترکیب غیر آلی است که به طور برگشت پذیر از یک پلیمر به یک مونومر در دمای ملایم تبدیل می شود.
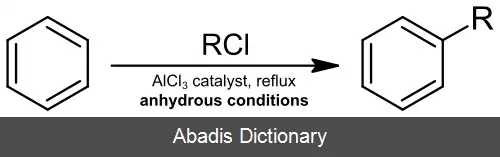
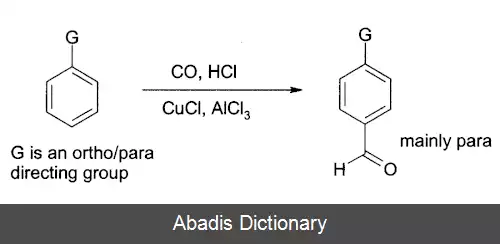
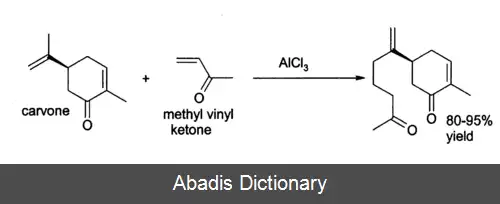
AlCl3 یک کاتالیزور رایج اسید لوئیس برای واکنشهای فریدل - کرفتس است ، هم آسیلاسیون و هم آلکیلاسیون. محصولات مهم شوینده ها و اتیل بنزن هستند. این نوع واکنش ها بیشترین کاربرد را برای کلرید آلومینیوم دارند ، به عنوان مثال ، در تهیه آنتراکینون ( مورد استفاده در صنایع مواد رنگی ) از بنزن و فسژن. [ ۳] در واکنش کلی فریدل - کرفتس ، یک آسیل کلراید یا آلکیل هالید با یک سیستم معطر واکنش نشان می دهد همانطور که نشان داده شده است:
واکنش آلکیلاسیون بیشتر از واکنش آسیلاسیون استفاده می شود ، اگرچه عملکرد آن از نظر فنی بیشتر طلب می کند. برای هر دو واکنش ، کلرید آلومینیوم و همچنین سایر مواد و تجهیزات باید خشک باشند ، اگرچه اثری از رطوبت است برای ادامه واکنش لازم است. روشهای تفصیلی برای آلکیلاسیون[ ۴] و آسیلاسیون عرصه ها در دسترس است.
یک مشکل کلی با واکنش فریدل - کرفتس این است که کاتالیزور کلرید آلومینیوم گاهی اوقات به مقدار کامل استوکیومتری مورد نیاز است ، زیرا به شدت با محصولات پیچیده می شود. این عارضه گاهی مقدار زیادی زباله خورنده تولید می کند. به همین دلیل و دلایل مشابه ، استفاده از کلرید آلومینیوم اغلب توسط زئولیت ها جابجا شده است[ ۲] .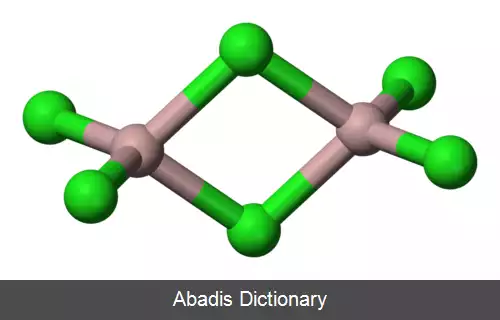
این نوشته برگرفته از سایت ویکی پدیا می باشد، اگر نادرست یا توهین آمیز است، لطفا گزارش دهید: گزارش تخلفکلرید آلومینیوم ( AlCl3 ) ، همچنین به عنوان تری کلرید آلومینیوم شناخته می شود ، ترکیباتی را با فرمول AlCl3 ( H2O ) n توصیف می کند ( n = 0یا 6 ) . آنها از اتمهای آلومینیوم و کلر به نسبت 1: 3 تشکیل شده اند و یک فرم نیز حاوی شش آب هیدراتاسیون است. هر دو ماده جامد سفید هستند ، اما نمونه ها اغلب با کلرید آهن ( III ) آلوده می شوند و به آنها رنگ زرد می دهد.
ماده بی آب از نظر تجاری مهم است. دارای نقطه ذوب و جوش کم است. این ماده عمدتاً در تولید فلز آلومینیوم تولید و مصرف می شود ، اما مقادیر زیادی نیز در سایر مناطق صنایع شیمیایی استفاده می شود. [ ۲] این ترکیب اغلب به عنوان اسید لوئیس ذکر می شود. این نمونه ای از یک ترکیب غیر آلی است که به طور برگشت پذیر از یک پلیمر به یک مونومر در دمای ملایم تبدیل می شود.
AlCl3 یک کاتالیزور رایج اسید لوئیس برای واکنشهای فریدل - کرفتس است ، هم آسیلاسیون و هم آلکیلاسیون. محصولات مهم شوینده ها و اتیل بنزن هستند. این نوع واکنش ها بیشترین کاربرد را برای کلرید آلومینیوم دارند ، به عنوان مثال ، در تهیه آنتراکینون ( مورد استفاده در صنایع مواد رنگی ) از بنزن و فسژن. [ ۳] در واکنش کلی فریدل - کرفتس ، یک آسیل کلراید یا آلکیل هالید با یک سیستم معطر واکنش نشان می دهد همانطور که نشان داده شده است:
واکنش آلکیلاسیون بیشتر از واکنش آسیلاسیون استفاده می شود ، اگرچه عملکرد آن از نظر فنی بیشتر طلب می کند. برای هر دو واکنش ، کلرید آلومینیوم و همچنین سایر مواد و تجهیزات باید خشک باشند ، اگرچه اثری از رطوبت است برای ادامه واکنش لازم است. روشهای تفصیلی برای آلکیلاسیون[ ۴] و آسیلاسیون عرصه ها در دسترس است.
یک مشکل کلی با واکنش فریدل - کرفتس این است که کاتالیزور کلرید آلومینیوم گاهی اوقات به مقدار کامل استوکیومتری مورد نیاز است ، زیرا به شدت با محصولات پیچیده می شود. این عارضه گاهی مقدار زیادی زباله خورنده تولید می کند. به همین دلیل و دلایل مشابه ، استفاده از کلرید آلومینیوم اغلب توسط زئولیت ها جابجا شده است[ ۲] .





wiki: آلومینیم کلرید
